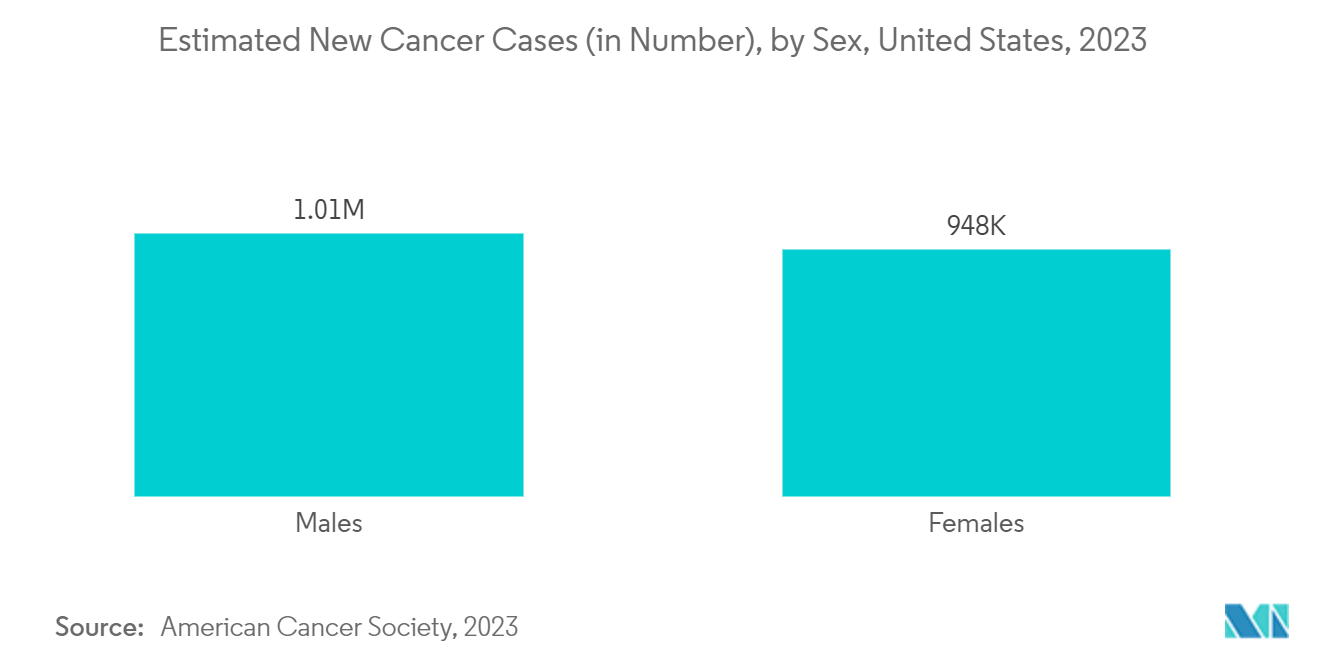| 研究期 | 2019 - 2029 |
| 估计的基准年 | 2023 |
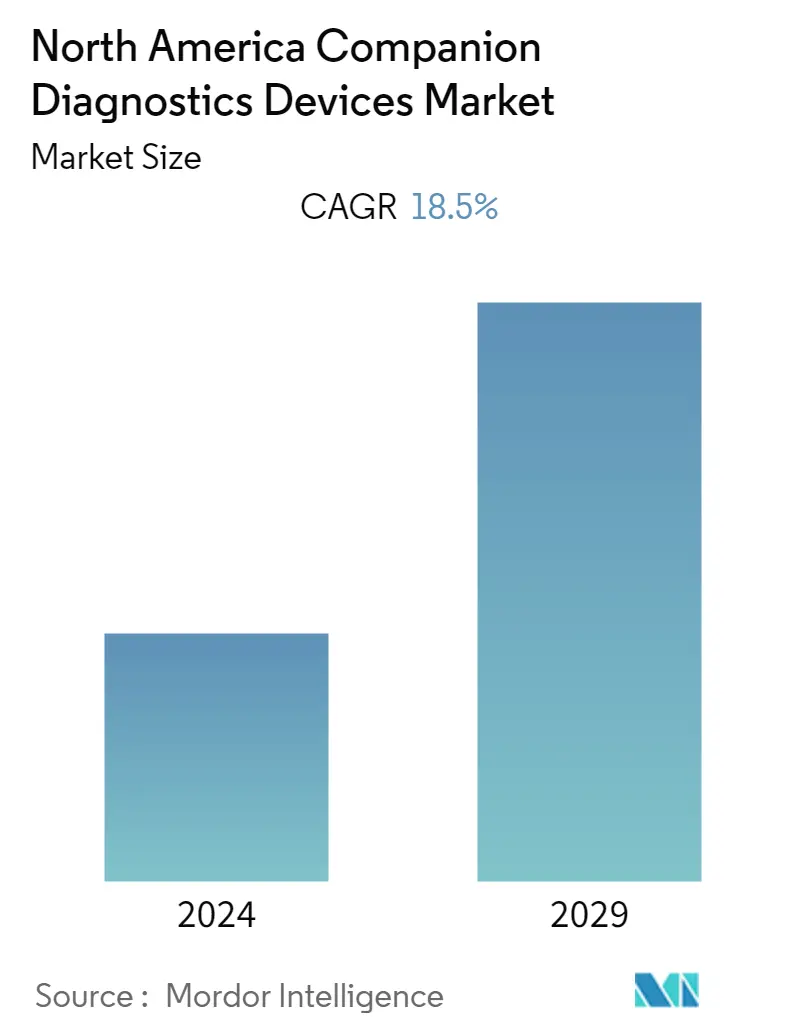
| CAGR | 18.50 % |
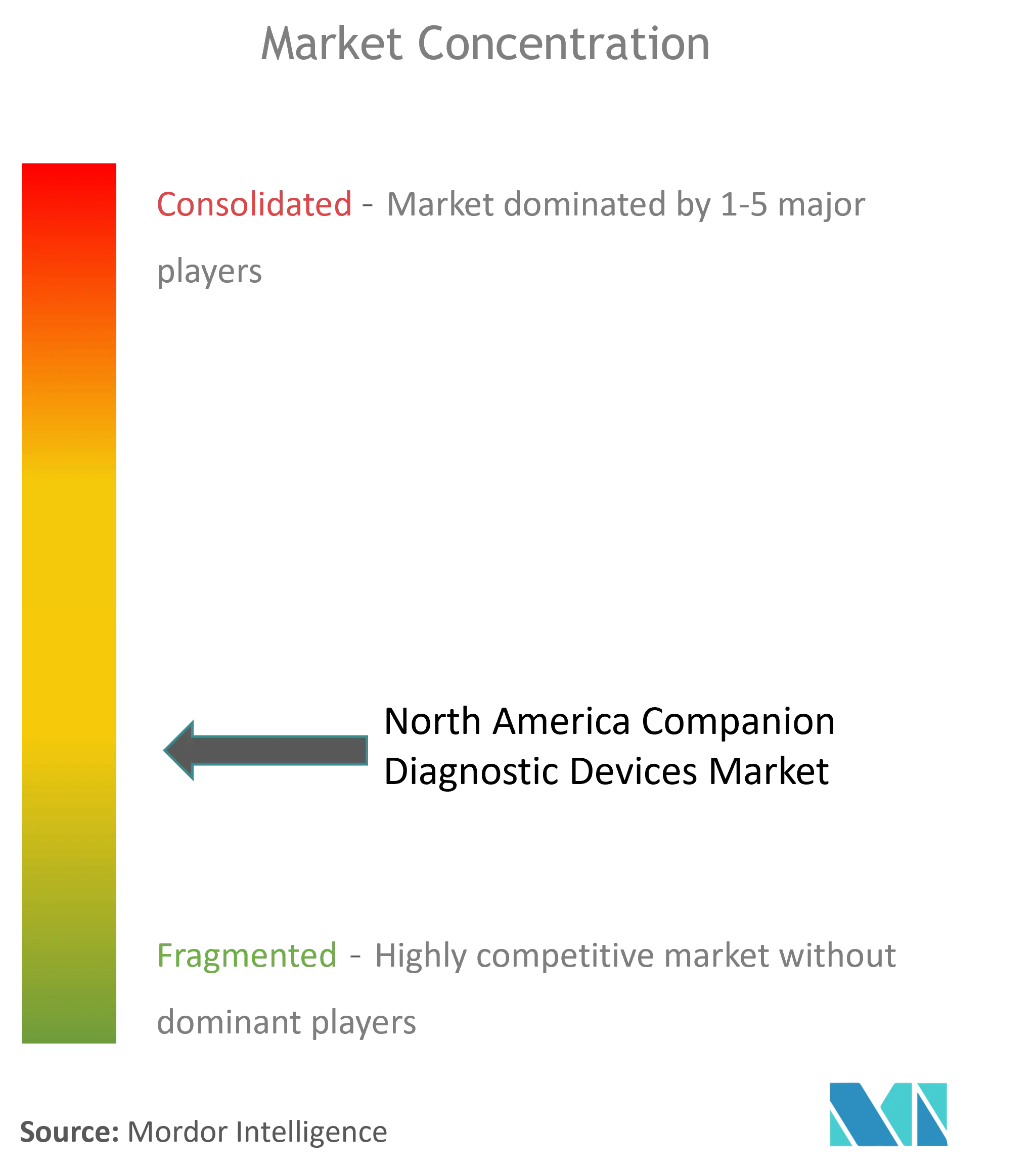
| 市场集中度 | 中等的 |
主要参与者*免责声明:主要玩家排序不分先后 |
北美伴随诊断设备市场分析
北美伴随诊断设备市场预计在预测期内复合年增长率为 18.5%。
COVID-19 影响了伴随诊断设备市场的增长。例如,根据药学系统评论2022 年 5 月发表的一篇文章,血清学抗体检测被用作 SARS-CoV-2 疫苗接种伴随诊断,以加强 COVID-19 免疫接种计划。此外,根据同一消息来源,SARS-CoV-2 疫苗接种伴随诊断具有多种优势,包括通过特定测试组合进行监测来提供持久、可靠的免疫保护,从而提供针对 COVID-19 的医疗安全。这增加了大流行期间对伴随诊断的需求。此外,新出现的新变异或耐药变异增加了对替代疗法和快速伴随诊断的需求,以对抗急性感染以及了解变异对健康的短期和长期影响。因此,所研究的市场已经出现显着增长,预计在预测期内还将增长。
对个性化药物和靶向治疗的需求和认识不断增加、药物不良反应病例增加以及设备技术进步等因素预计将在预测期内推动市场增长。
这家不断成长的公司专注于采用各种关键策略,例如协作、伙伴关系等,以改善个性化药物的获取,以及提高人群对靶向治疗的认识,预计将增加伴随诊断测试的采用。预计这将推动市场增长。例如,2021 年 5 月,加拿大霍夫曼罗氏有限公司与 BC Cancer 和加拿大个性化医疗创新网络 (CPHIN) 签署了一项联合倡议,在不列颠哥伦比亚省共同创建真实世界证据 (RWE) 框架。 PREDiCT 计划生成并评估 RWE,可用于为个性化癌症治疗制定新的可持续报销途径。
此外,靶向治疗研究和开发的激增预计也将增加对伴随诊断测试和设备的需求,从而促进市场增长。例如,2021年5月,美国FDA批准Rybrevant(amivantamab)作为靶向治疗药物,用于治疗肿瘤具有表皮生长因子受体(EGFR)外显子20插入突变的成年非小细胞肺癌患者。
此外,公司在开发技术先进产品方面的活动不断增长,以及新产品的推出和批准的增加,预计也将在预测期内促进该地区的市场增长。例如,2021 年 7 月,Labcorp 推出了 therascreen KRAS PCR 突变分析,这是一种伴随诊断,用于识别适合接受 LUMAKRAS (sotorasib) 治疗的非小细胞肺癌 (NSCLC) 患者。同样,2021 年 5 月,QIAGEN NV 在美国推出了 therascreen KRAS RGQ PCR 试剂盒的伴随诊断 (CDx) 范围扩大声明,作为伴随诊断来帮助识别非小细胞肺癌 (NSCLC) 患者可能有资格接受 LUMAKRAST 批准的治疗。
因此,由于上述因素,预计所研究的市场将在预测期内增长。然而,药物开发和相关临床试验的高成本可能会阻碍预测期内伴随诊断设备市场的增长。
北美伴随诊断设备市场趋势
原位杂交 (ISH) 领域预计将在预测期内呈现最快的增长率
由于乳腺癌病例负担增加、人们对乳腺癌的认识不断增强以及新产品批准增加等因素,预计在预测期内,乳腺癌细分市场的伴随诊断设备市场将出现显着增长。
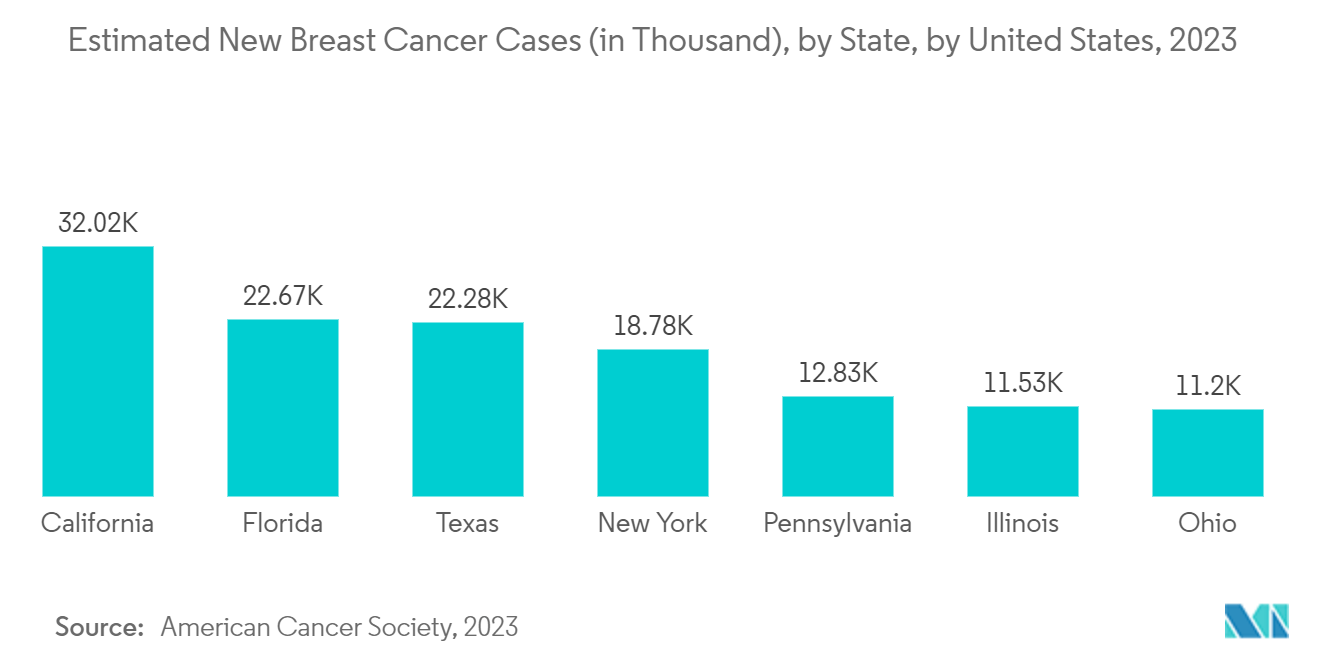
人群中乳腺癌发病率和患病率的增加提出了对有效和安全地施用药物或生物制品来治疗乳腺癌的需求,而这只有通过伴随诊断设备才能实现,从而推动市场增长。例如,根据加拿大癌症协会2022年5月发布的统计数据,乳腺癌是最常见的恶性肿瘤,也是加拿大女性癌症相关死亡的第二大原因。根据同一来源,预计 2022 年将有 28,600 名加拿大女性被诊断出患有乳腺癌,占 2022 年女性所有新癌症病例的 25%。此外,根据 ACS 发布的 2023 年统计数据,大约有 297,790 名新乳腺癌病例预计 2023 年美国将诊断出 55,720 例新的浸润性乳腺癌和导管原位癌 (DCIS) 病例。
此外,新产品批准量的增加增加了该地区先进诊断设备的可用性,预计这也将推动该领域在预测期内的增长。例如,2022 年 10 月,罗氏的 PATHWAY 抗 HER2/neu (4B5) 兔单克隆一抗获得美国 FDA 批准,这是第一个伴随诊断,用于识别 HER2 低表达的转移性乳腺癌患者,Enhertu (fam-曲妥珠单抗 deruxtecan-nxki)可被视为靶向治疗。
因此,由于上述因素,例如乳腺癌的高负担和新产品推出的增加,预计所研究的市场将在预测期内增长。
预计美国在预测期内将占据重要的市场份额
由于癌症负担不断增加、对个性化药物和靶向治疗的需求不断增长、高医疗保健支出和设备技术不断进步。
该国各种类型癌症的发病率和患病率不断增加,提出了早期发现癌症和诊断病情的需求。预计这将推动该国市场的增长。例如,根据 ACS 发布的 2023 年统计数据,预计 2023 年美国将诊断出约 1,958,310 例新癌症病例。此外,根据同一来源,预计将新增 238,340 例肺癌病例、153,020 例新结肠/直肠癌病例癌症病例, 预计 2023 年美国将诊断出 297,790 例乳腺癌病例。
此外,不断增加的新产品发布和产品批准增加了该国新型诊断设备的可用性,从而推动了市场增长。例如,2022 年 8 月,美国 FDA 批准 Thermo Fisher Scientific 的 Oncomine Dx Target 测试作为伴随诊断 (CDx),以帮助识别肿瘤携带表皮生长因子受体的非小细胞肺癌 (NSCLC) 患者。 EGFR)Exon20 插入突变可用于 RYBREVANT 靶向治疗的潜在治疗。此外,2021 年 10 月,美国 FDA 批准了安捷伦的 Ki-67 IHC MIB-1 pharmDx (Dako Omnis),该产品有助于识别疾病复发高风险的早期乳腺癌 (EBC) 患者。
因此,由于上述因素,例如癌症的高负担和新产品的推出,预计所研究的市场在预测期内将在美国增长。
北美伴随诊断设备行业概述
由于存在大量参与者,北美伴随诊断设备市场竞争非常激烈。市场上的一些主要公司包括 Abbott Laboratories、Agilent Technologies Inc.、Biomerieux SA、F. Hoffmann-La Roche Ltd、Qiagen NV、Siemens Healthcare 和 Thermo Fisher Scientific Inc. 等。
北美伴随诊断设备市场领导者
-
Abbott
-
F. Hoffmann-La Roche Ltd
-
Biomerieux SA
-
Qiagen NV
-
Agilent Technologies Inc.
- *免责声明:主要玩家排序不分先后
北美伴随诊断设备市场新闻
- 2023 年 1 月,QIAGEN 与 Helix o 建立独家战略合作伙伴关系,针对心血管、代谢、神经退行性疾病、自身免疫性疾病等遗传性疾病进行高级伴随诊断。根据协议条款,QIAGEN 将成为 Helix 伴随诊断服务在美国的独家营销和承包合作伙伴。
- 2022 年 12 月,QIAGEN 的therascreen KRAS RGQ PCR 试剂盒获得美国 FDA 批准 ,作为 Mirati Therapeutic 治疗非小细胞肺癌 (NSCLC) 的药物 KRAZATI (adagrasib) 的伴随诊断测试。
北美伴随诊断设备行业细分
根据报告的范围,伴随诊断测试提供对于安全有效使用相应药物或生物制品至关重要的信息。北美伴随诊断设备市场按技术(免疫组织化学(IHC)、聚合酶链反应(PCR)、原位杂交(ISH)、实时PCR(RT-PCR)、基因测序和其他技术)细分,适应症(肺癌、乳腺癌、结直肠癌、白血病、黑色素瘤和其他适应症)和地理。该报告提供了上述细分市场的价值(以百万美元为单位)。
| 技术 | 免疫组织化学 (IHC) | ||
| 聚合酶链式反应 (PCR) | |||
| 原位杂交 (ISH) | |||
| 实时荧光定量PCR (RT-PCR) | |||
| 基因测序 | |||
| 其他技术 | |||
| 指示 | 肺癌 | ||
| 乳腺癌 | |||
| 结直肠癌 | |||
| 白血病 | |||
| 黑色素瘤 | |||
| 其他适应症 | |||
| 地理 | 北美 | 美国 | |
| 加拿大 | |||
| 墨西哥 | |||
北美伴随诊断设备市场研究常见问题解答
目前北美伴随诊断设备市场规模有多大?
北美伴随诊断设备市场预计在预测期内(2024-2029 年)复合年增长率为 18.5%
谁是北美伴随诊断设备市场的主要参与者?
Abbott、F. Hoffmann-La Roche Ltd、Biomerieux SA、Qiagen NV、Agilent Technologies Inc. 是北美伴随诊断设备市场的主要公司。
该北美伴随诊断设备市场涵盖哪些年份?
该报告涵盖了北美伴随诊断设备市场历年市场规模:2019年、2020年、2021年、2022年和2023年。该报告还预测了北美伴随诊断设备市场历年规模:2024年、2025年、2026年、2027年、2028年和 2029 年。
我们最畅销的报告
Popular Animal Health Reports
Popular Healthcare Reports
北美伴随诊断设备行业报告
Mordor Intelligence™ 行业报告创建的 2024 年北美伴随诊断设备市场份额、规模和收入增长率统计数据。北美伴侣诊断设备分析包括 2024 年至 2029 年的市场预测展望和历史概述。获取此行业分析的样本(免费下载 PDF 报告)。