| Período de Estudo | 2019 - 2029 |
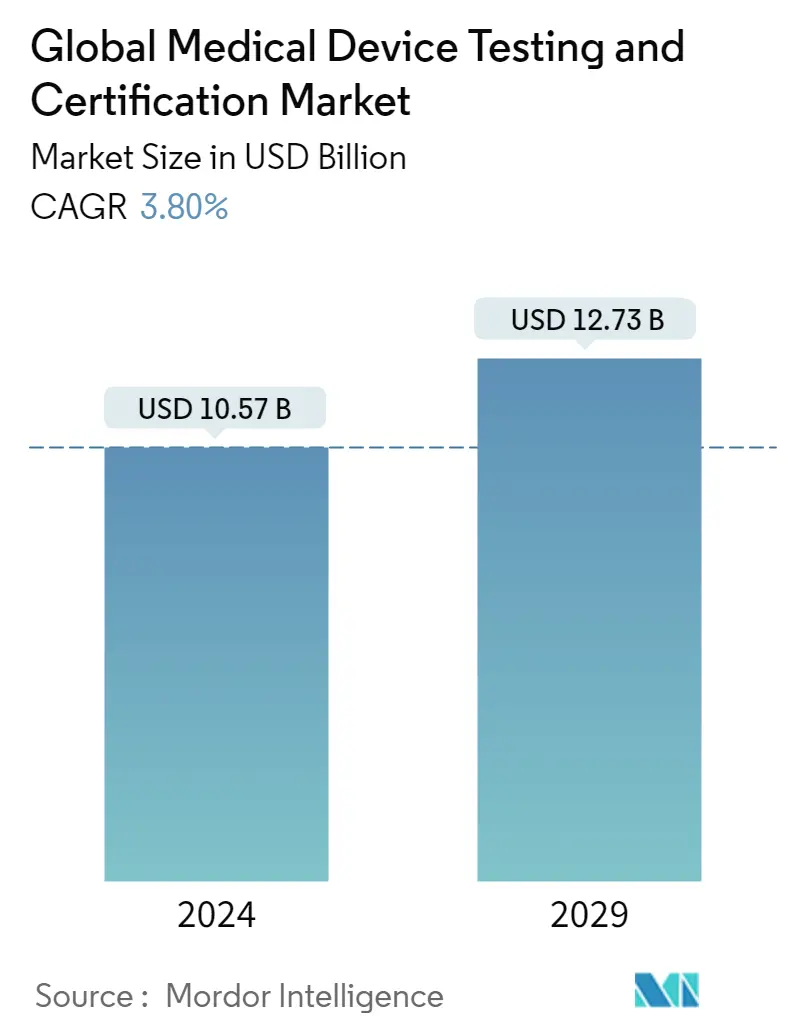
| Tamanho do Mercado (2024) | USD 10.55 Billion |
| Tamanho do Mercado (2029) | USD 12.71 Billion |
| CAGR (2024 - 2029) | 3.80 % |
| Mercado de Crescimento Mais Rápido | Ásia-Pacífico |
| Maior Mercado | América do Norte |
| Concentração do Mercado | Baixo |
Principais jogadores*Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica |
Análise de mercado de testes de dispositivos médicos
O tamanho do mercado global de testes e certificação de dispositivos médicos é estimado em US$ 10,57 bilhões em 2024 e deve atingir US$ 12,73 bilhões até 2029, crescendo a um CAGR de 3,80% durante o período de previsão (2024-2029).
Durante o surto de COVID-19 em 2020, diversas medidas foram tomadas para prevenir a transmissão de doenças, como medidas de bloqueio e restrição das atividades de importação e exportação entre os países, o que interrompeu a cadeia de abastecimento, impactando negativamente o mercado geral estudado.
Além disso, a perturbação causada pela COVID-19 nas cadeias de abastecimento internacionais levou à escassez de dispositivos médicos críticos em todo o mundo. Portanto, muitos países tomaram medidas definitivas para aliviar a escassez através da importação de equipamentos, tais como a produção nacional de dispositivos médicos. Além disso, espera-se que a fabricação nacional de dispositivos médicos essenciais supere as barreiras comerciais e, ao mesmo tempo, garanta a qualidade do produto e a estabilidade do mercado.
De acordo com o British Standards Institution (BSI), em fevereiro de 2020, levando em consideração os efeitos da pandemia COVID-19, a empresa revisou processos e planejou um programa para minimizar o risco para clientes e colegas do British Standards Institution (BSI), mantendo ao mesmo tempo requisitos de acreditação e mitigação de potenciais riscos comerciais globais.
Os dispositivos médicos estão sujeitos ao cumprimento de protocolos regulatórios rigorosos, pois é vital garantir a eficácia e segurança dos dispositivos médicos. Portanto, é obrigatório que todos os dispositivos cumpram as normas nacionais e internacionais antes de entrar no mercado. As diretrizes padrão de dispositivos médicos variam de país para país e é obrigatório que todos os fabricantes sigam essas diretrizes para comercializar ou vender seus produtos em um país. Por exemplo, os Estados Unidos seguem as diretrizes da Food and Drug Administration (FDA), a Europa considera a aprovação da Conformitè Europëenne (CE), o Canadá precisa do registro da Health Canada e a Índia exige a aprovação da Central Drugs Standard Control Organization (CDSCO). Esta gama diversificada de cenários regulatórios impulsiona o mercado de testes e certificação.
Uma vez que os regulamentos são diferentes em cada país, é crucial que cada fabricante de dispositivos médicos registe ou receba diretrizes regulamentares desse país específico, o que, por sua vez, indica a necessidade de terceiros autorizados registarem os seus dispositivos. As autoridades reguladoras nacionais de cada país preferem que os fabricantes que vendem os seus produtos nesse país específico cumpram as diretrizes padrão e sejam verificados por um sistema de certificação de terceiros.
Isto pode resultar no impulso do mercado de testes e certificação, bem como no aumento do acesso fácil ao mercado. Os outros fatores, como a crescente necessidade de validação e verificação (VV) para dispositivos médicos, estão impulsionando o mercado de testes e certificação de dispositivos médicos. No entanto, espera-se que um fator como a diversidade na regulamentação impeça o crescimento do mercado durante o período de previsão.
Tendências do mercado de testes de dispositivos médicos
Espera-se que o segmento de serviços de teste testemunhe um rápido crescimento durante o período de previsão
Globalmente, os dispositivos médicos são regulamentados por diversas autoridades reguladoras e de conformidade. Isto ocorre principalmente porque os usuários finais desses dispositivos esperam excelente desempenho, eficácia e segurança desses dispositivos médicos. Portanto, é obrigatório que os fabricantes definam e implementem adequadamente uma estratégia de teste de dispositivos médicos, o que torne o dispositivo eficaz e a produção seja mais fácil devido à confirmação da qualidade.
Em abril de 2020, devido à pandemia de COVID-19, a Comissão Europeia (CE) adotou uma proposta para adiar por um ano a data de aplicação do Regulamento sobre Dispositivos Médicos (MDR) porque a pandemia de COVID-19 aumentou a procura de determinados dispositivos médicos, que foram cruciais para evitar riscos ou dificuldades de potencial escassez de tais dispositivos. Além disso, a pandemia da COVID-19 atrasou os ensaios clínicos e interrompeu os processos relativos aos dispositivos médicos.
Alguns dos dispositivos médicos sofreram um aumento repentino na demanda durante a pandemia de COVID-19 de 2020. Por exemplo, os ventiladores tiveram alta demanda para pacientes com COVID-19, pois são uma ferramenta importante em hospitais que podem manter vivos os pacientes em condições críticas.. Por exemplo, em Março de 2020, a Medtronic PLC anunciou que tinha aumentado a produção em mais de 40% até à data e estava no bom caminho para mais do que duplicar a sua capacidade de fabricar e fornecer ventiladores em resposta às necessidades urgentes dos pacientes e dos sistemas de saúde em todo o mundo. mundo que enfrenta a COVID-19.
Em junho de 2020, o Intertek Group PLC anunciou a expansão dos serviços de equipamentos de proteção individual para incluir testes de respiradores N95 de acordo com os requisitos estabelecidos pelo Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH). Com esta expansão, a empresa também expandiu as suas soluções e recursos para apoiar os clientes e a comunidade global durante a pandemia da COVID-19.
Uma estratégia eficaz de testes de dispositivos médicos necessita de vários conjuntos de requisitos de teste. Os conjuntos de requisitos são necessários para facilitar a implementação dos testes, uma vez que os testes são realizados continuamente em diferentes estágios do processo completo de fabricação, desde a seleção dos componentes até a montagem final de um dispositivo médico. Cada estágio possui requisitos diferentes e parâmetros diferentes a serem satisfeitos. Assim, o aumento dos dispositivos médicos também pode aumentar estes serviços de testes, o que deverá aumentar o crescimento global do mercado.
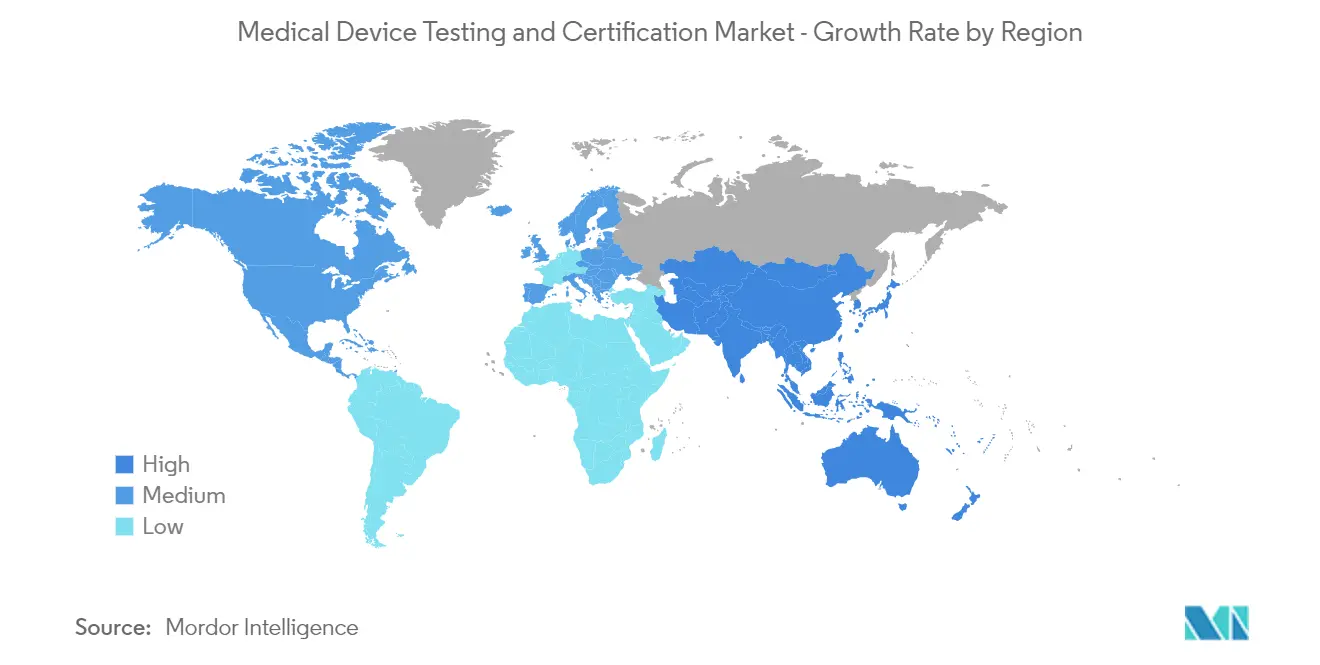
A América do Norte domina o mercado e espera-se que faça o mesmo durante o período de previsão
Alguns dos fatores que impulsionam o crescimento do mercado na região norte-americana incluem o aumento do foco na qualidade dos dispositivos médicos e a presença de um grande número de empresas que atendem a indústria de dispositivos médicos, juntamente com a presença de cuidados de saúde bem desenvolvidos e o presença das principais empresas multinacionais de dispositivos médicos.
De acordo com um artigo de pesquisa de A. Chandimal Nicholas publicado em maio de 2020, no Canadá, durante a pandemia de COVID-19 de 2020, o Ministro da Saúde assinou a Ordem Provisória Respeitando a Importação e Venda de Dispositivos Médicos para Uso em relação ao COVID-19 , que permitiu acesso rápido a dispositivos médicos COVID-19 para uso por prestadores de cuidados de saúde. Além disso, de acordo com a Health Canada, a Ordem Provisória ajudou na rápida aprovação da importação e venda de dispositivos médicos COVID-19.
Além disso, durante a pandemia de COVID-19 de 2020, nos Estados Unidos, a Food and Drug Administration (FDA) emitiu autorizações de uso de emergência (EUA) para dispositivos médicos para diagnosticar a COVID-19 e equipamentos de proteção individual necessários para proteger os profissionais de saúde que interagem com os pacientes.
Nos Estados Unidos, os dispositivos médicos são geridos pela Food and Drug Administration (FDA) para garantir a segurança e eficácia dos dispositivos. O Centro de Dispositivos e Saúde Radiológica (CDRH) é um segmento da Food and Drug Administration (FDA). Os dispositivos de Classe II exigem controles notáveis para rotulagem, orientação, rastreamento, planejamento, padrões de desempenho e observação pós-comercialização, e a maioria exige notificação pré-comercialização 510(k) para avaliar a equivalência substancial a um dispositivo comercializado legalmente.
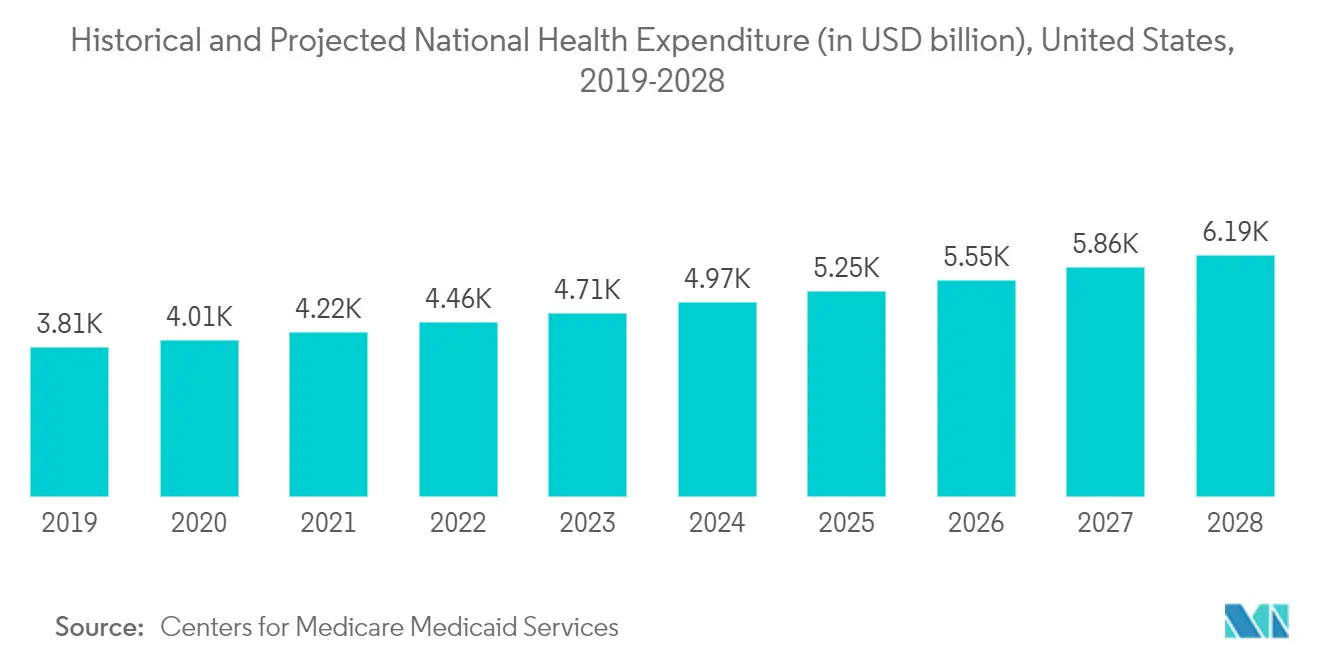
De acordo com o Center for Medicare Medicaid Services, os gastos com saúde nos Estados Unidos cresceram 4,6% em 2018, atingindo 3,6 biliões de dólares ou 11.172 dólares por pessoa. Como parcela do Produto Interno Bruto do país, os gastos com saúde representaram 17,7%. Além disso, com o aumento da aprovação de dispositivos médicos na região, o aumento da demanda por serviços de testes de dispositivos médicos pode impulsionar o crescimento do mercado. Assim, considerando os fatores acima mencionados, espera-se que alimente o crescimento do mercado na região norte-americana durante o período de previsão.
Visão geral da indústria de testes de dispositivos médicos
O mercado de testes e certificação de dispositivos médicos é altamente consolidado e poucas empresas prestam serviços de testes e certificação. Observou-se que, com o crescente mercado de dispositivos médicos, espera-se que mais empresas entrem no mercado no futuro. Uma participação de mercado substancial poderá ser conquistada pelas pequenas e médias empresas nos próximos anos. Alguns participantes do mercado incluem BSI Group, Intertek Group PLC, Institute for Testing and Certification Inc., Eurofins Scientific e SGS SA, entre outros.
Líderes de mercado de testes de dispositivos médicos
-
Eurofins Scientific
-
Institute for Testing and Certification Inc.
-
BSI Group
-
SGS SA
-
Intertek Group PLC
- *Isenção de responsabilidade: Principais participantes classificados em nenhuma ordem específica
Notícias do mercado de testes de dispositivos médicos
- Em janeiro de 2022, a TÜV SÜD expandiu seu laboratório de testes de dispositivos médicos em New Brighton, Minnesota. O laboratório de última geração fornecerá uma ampla gama de testes químicos e biológicos de dispositivos médicos que complementam as atuais capacidades de testes ativos de dispositivos médicos da TÜV SÜD.
- Em janeiro de 2022, a DNV, fornecedora global de certificação, garantia e gerenciamento de risco, adquiriu a MEDCERT para expandir sua presença em garantia de dispositivos médicos.
Segmentação da indústria de testes de dispositivos médicos
De acordo com o escopo do relatório, testes, certificação e auditoria de dispositivos médicos são necessários para garantir a segurança dos dispositivos. Esses testes e certificação podem ser fornecidos por terceiros sob a organização de auditoria reconhecida. O mercado global de testes e certificação de dispositivos médicos é segmentado por tipo de serviço (serviços de teste, serviços de inspeção, serviços de certificação e outros serviços), tipo de fornecimento (interno e terceirizado), classe de dispositivo (classe I, classe II e classe III ), tecnologia (dispositivo médico de implante ativo, dispositivo médico ativo, dispositivo médico não ativo, dispositivo médico para diagnóstico in vitro, dispositivo médico oftalmológico, dispositivo médico ortopédico e odontológico e outras tecnologias) e geografia (América do Norte, Europa, Ásia-Pacífico , Oriente Médio e África e América do Sul). O relatório oferece o valor (em milhões de dólares) para os segmentos acima.
| Por tipo de serviço | Serviços de teste | ||
| Serviços de inspeção | |||
| Serviços de certificação | |||
| Outros serviços | |||
| Por tipo de fornecimento | Interno | ||
| Terceirizado | |||
| Por classe de dispositivo | Classe I | ||
| Classe II | |||
| Classe III | |||
| Por tecnologia | Dispositivo médico de implante ativo | ||
| Dispositivo Médico Ativo | |||
| Dispositivo médico não ativo | |||
| Dispositivo médico de diagnóstico in vitro | |||
| Dispositivo médico oftálmico | |||
| Dispositivo Médico Ortopédico e Odontológico | |||
| Outras tecnologias | |||
| Por geografia | América do Norte | Estados Unidos | |
| Canadá | |||
| México | |||
| Europa | Alemanha | ||
| Reino Unido | |||
| França | |||
| Itália | |||
| Espanha | |||
| Resto da Europa | |||
| Ásia-Pacífico | China | ||
| Japão | |||
| Índia | |||
| Austrália | |||
| Coreia do Sul | |||
| Resto da Ásia-Pacífico | |||
| Oriente Médio e África | CCG | ||
| África do Sul | |||
| Resto do Médio Oriente e África | |||
| América do Sul | Brasil | ||
| Argentina | |||
| Resto da América do Sul | |||
Perguntas frequentes sobre pesquisa de mercado de testes de dispositivos médicos
Qual é o tamanho do mercado global de testes e certificação de dispositivos médicos?
O tamanho do mercado global de testes e certificação de dispositivos médicos deve atingir US$ 10,57 bilhões em 2024 e crescer a um CAGR de 3,80% para atingir US$ 12,73 bilhões até 2029.
Qual é o tamanho atual do mercado global de testes e certificação de dispositivos médicos?
Em 2024, o tamanho do mercado global de testes e certificação de dispositivos médicos deverá atingir US$ 10,57 bilhões.
Quem são os principais atores do mercado global de testes e certificação de dispositivos médicos?
Eurofins Scientific, Institute for Testing and Certification Inc., BSI Group, SGS SA, Intertek Group PLC são as principais empresas que operam no mercado global de testes e certificação de dispositivos médicos.
Qual é a região que mais cresce no mercado global de testes e certificação de dispositivos médicos?
Estima-se que a Ásia-Pacífico cresça no maior CAGR durante o período de previsão (2024-2029).
Qual região tem a maior participação no mercado global de testes e certificação de dispositivos médicos?
Em 2024, a América do Norte é responsável pela maior participação de mercado no mercado global de testes e certificação de dispositivos médicos.
Que anos esse mercado global de testes e certificação de dispositivos médicos cobre e qual era o tamanho do mercado em 2023?
Em 2023, o tamanho do mercado global de testes e certificação de dispositivos médicos foi estimado em US$ 10,18 bilhões. O relatório abrange o tamanho histórico do mercado global de testes e certificação de dispositivos médicos para anos 2019, 2020, 2021, 2022 e 2023. O relatório também prevê o tamanho do mercado global de testes e certificação de dispositivos médicos para anos 2024, 2025, 2026, 2027 , 2028 e 2029.
Nossos relatórios mais vendidos
Popular Health Services Reports
Popular Healthcare Reports
Relatório da indústria de testes de dispositivos médicos
Estatísticas para a participação de mercado de testes de dispositivos médicos em 2024, tamanho e taxa de crescimento de receita, criadas por Mordor Intelligence™ Industry Reports. A análise de testes de dispositivos médicos inclui uma perspectiva de previsão de mercado para 2029 e uma visão geral histórica. Obtenha uma amostra desta análise do setor como um download gratuito em PDF do relatório.