マーケットトレンド の 医薬品開発製造受託機関(CDMO) 産業
研究開発投資の増加が市場を牽引
- 米国は最大の医薬品市場の一つであり、医薬品・バイオテクノロジー市場における研究開発費の約半分を占めている。CMOはこの市場で重要な役割を担っており、さまざまなアウトソーシング先にサービスを提供するため、新しい施設や技術に投資している。さらに、企業は自社投資を通じてアジアでの事業展開のメリットを享受するだけでなく、ハイエンドの調達専門知識の獲得、創薬の構築、投資のために研究ベースの提携も模索している。
-
- 例えば、2024年1月、ベルギーのバイオテクノロジー企業であるEXO Biologics SAは、アンメット・メディカル・ニーズの高い希少疾患の治療にエクソソームを利用したバイオ医薬品の開発に取り組んでおり、エクソソームに特化した開発・製造受託機関(CDMO)であるExoXpertを立ち上げた。ExoXpertは、欧州の臨床試験で使用されているMSCベースのエクソソーム製造プラットフォームを提供しており、EXO Biologicsの完全子会社である。
- 製薬会社のターゲットが科学研究と医薬品マーケティングにシフトする中、CDMOは重要なパートナーとしての地位をさらに確立し、顧客との戦略的で統合的なパートナーシップを構築することができる。
- 複雑で高力価の化合物が増加する中、CDMOは高度な技術と専門的な専門知識によって際立つことができる。さらに、連続製造などの新たな業務アプローチにより、CDMOは製造プロセスの効率を向上させ、コストと無駄を削減できると期待されている。
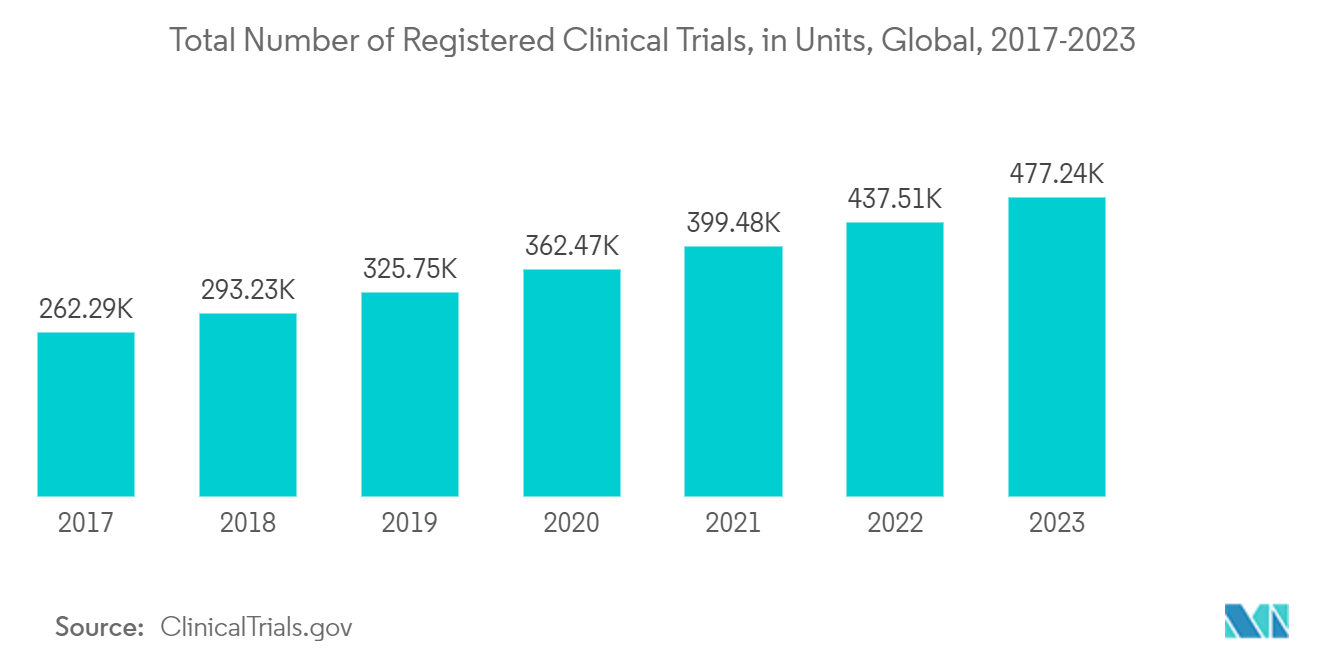
- さらに、市場は臨床試験の成長を目の当たりにしており、需要を牽引している。例えば、ClinicalTrials.govによると、登録された臨床試験の総数は2022年に4億3,751万3,000件で、2023年には4億7,723万7,000件に達する。
- CDMOは、増加する中小製薬企業と新たな機会を見出すと予想される。このような中小製薬会社は、主に新薬承認件数の増加の原因となっており、製造能力を持たないことが多い。
アジア太平洋地域はCRO分野で最も急成長する地域と予想される
- アジア太平洋地域は、米国や他の先進国に比べて低コストであるため、予測期間中に CRO 市場が最も高成長すると予想される。加えて、糖尿病や心臓病などの慢性疾患や生活習慣病の罹患率の増加、患者募集の容易さ、臨床試験のための専門知識の利用可能性などが、この地域の成長を後押しする主な原動力となっている。
- 例えば、国家衛生委員会(NHC)によると、中国には慢性疾患に苦しむ高齢者が1億8,000万人以上おり、そのうち75%が複数の慢性疾患に罹患している。2030年までに、心血管疾患は中国政府に1兆440億米ドルの損失をもたらすと予測されている。糖尿病有病率の高さについては、中国、韓国、オーストラリアを含むアジア太平洋地域でも同様の傾向が見られる。
- 臨床試験の民営化が進むにつれ、中国やインドなどの発展途上国では研究プロセスのアウトソーシングが増加している。例えば、大手製薬会社は臨床データ管理、ファーマコビジランス、生物統計学などの研究サービスをアウトソーシングするケースが増えている。
- 特定の地域が臨床試験を実施する組織を惹きつける理由は数多くある。その中には、コスト、患者の募集、必要な試験、スケジュールの短縮などが含まれる。中国、インド、日本では臨床試験の数が全体的に増加しており、アジア太平洋地域は潜在的な地域の一つとなっている。
- インドは先進国よりも低コストで前臨床サービスを提供している。CRO の可能性を拡大するためにインド政府が行ったイニシアチブは、近年魅力的な市場機会を提供している。
- インドでは科学的な専門知識が利用可能であるため、今後数年間はビジネスの成長を後押しする可能性がある。インドにおける臨床試験のコストは、米国よりも約 50%低い。インドは最大級の医薬品生産国であり、米国以外では最も多くのFDA承認製造工場を持っているため、中国に対する競争力がある。