マーケットトレンド の コンパニオン診断 産業
肺がん分野は予測期間中に著しい成長が見込まれる
コンパニオン診断検査(CDX)は、肺癌における標的療法による治療の意思決定において必須であると考えられている。初回治療の一環としてコンパニオン診断検査を受けた肺がん患者は、標的治療の選択など、より多くの生存利益を得ることができ、対象患者に個別化された治療を提供するのに役立つ
肺がんの罹患率の高さと、主要企業によるコンパニオン診断薬の新たな技術革新が、予測期間中の同分野の成長を後押しすると思われる
世界的には、非小細胞肺がん(NSCLC)の罹患率の高さと、この疾患に対する腫瘍学コンパニオン診断検査の開発の進展が、同分野の成長を押し上げると予想されている。例えば、2024年1月に米国癌協会が発表した報告書によると、肺癌全体の約10〜15%が小細胞肺癌(SCLC)であり、約80〜85%が非小細胞肺癌(NSCLC)であった。同じ情報源によると、米国では2024年に234,580人が新たに肺癌に罹患すると推定されており、肺癌コンパニオン診断薬の需要が高まっている。同様に、米国癌協会が2023年に発表した報告書によると、約238,340人が肺癌と診断された。このような有病率は、コンパニオン診断市場における肺がん分野の予測期間中の成長を促進すると予想される
また、同分野は、製品の承認数や発売数の増加によっても成長している。2023年6月、ARUP Laboratories社は、ROCTAVIAN(valoctocogene roxaparvovec-rvox)による治療の対象となる成人患者の選択を支援するコンパニオン診断薬として、AAV5 DetectCDxの承認を米国食品医薬品局から取得した
各社はまた、市場における製品ポートフォリオを拡大するため、主要な提携戦略の採用にも注力している。2023年7月、TempusはTScan Therapeuticsと提携し、がん患者を治療するためのコンパニオン診断(CDx)検査を開発した。この提携は、非小細胞肺癌を含む固形癌のフェーズ1におけるTScan社のスクリーニング・プロトコルをサポートするもので、腫瘍抗原陽性とインタクトなHLA発現に基づいてカスタマイズされた混合TCR-Tを患者に投与できるように設計された臨床試験である
したがって、肺がんの罹患率の高さ、大手企業によるコンパニオン診断における新たなイノベーション、戦略的活動が、予測期間中の同分野の成長を促進すると予想される
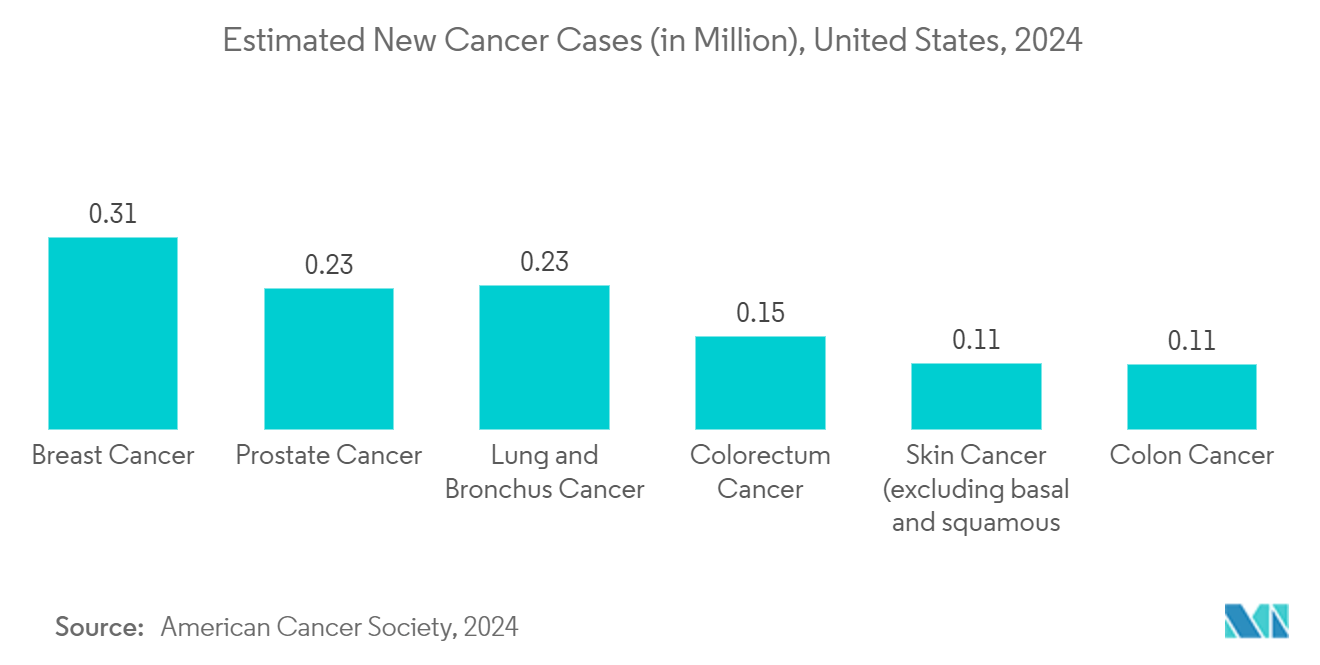
予測期間中、北米が大きな市場シェアを占める見込み
北米はコンパニオン診断薬市場全体において大きな成長が見込まれており、米国が主要な貢献国として浮上している。コンパニオン診断薬は、FDAが関連するリスクに基づいてこれらのアッセイを分類していることからも明らかなように、様々な癌治療薬に関連する治療方針を決定するための極めて重要なツールとして認識されている。この認識は、癌領域におけるコンパニオン診断薬の戦略的重要性を強調し、十分な情報に基づいたリスク評価による治療方針の決定における重要な要素としてのコンパニオン診断薬の役割を強調しています
米国におけるがん罹患率の増加も市場を牽引すると予想される。例えば、Cancer Journal for Clinicians1が2024年1月に発表した報告書によると、米国では2024年に約313,510人の乳がん患者、152,810人の大腸がん患者、66,440人の膵臓がん患者が発生すると推定されている。カナダでも癌の罹患率が上昇しており、コンパニオン診断薬市場の需要を押し上げると期待されている。例えば、Canadian Cancer Statisticsが2023年11月に発表した報告書によると、カナダでは2022年に233,900件の新規がん症例が診断されたのに対し、2023年には約239,100件の新規がん症例が診断されると推定されている。このデータは、同地域における癌の負担が増加していることを示しており、コンパニオン診断薬の需要を押し上げると予想される
製品上市、戦略的提携、パートナーシップ、政府による製品承認が、予測期間中の北米コンパニオン診断薬市場を牽引すると期待されている。2023年6月、米国FDAは、臨床医が患者に適切ながん治療を選択できるように、特定のがん治療薬と対応する特定の体外診断用医薬品を使用する新たな自主的パイロットプログラムを開始した。同様に、2022年6月、ヘルスケア企業のGRAIL LLCは、アストラゼネカの治療薬と併用するコンパニオン診断(CDx)アッセイを開発・商業化するための戦略的提携をアストラゼネカと締結した。同社は、高リスクの早期疾患を有する患者を同定するコンパニオン診断薬の開発に注力している。このような開発は地域市場の成長にプラスの影響を与えると予想される
がん罹患率の増加、製品上市の増加、主要企業による成長戦略は、コンパニオン診断薬世界市場における同地域のシェアを大幅に押し上げると予想される