臨床試験市場規模・シェア
モードーインテリジェンスによる臨床試験市場分析
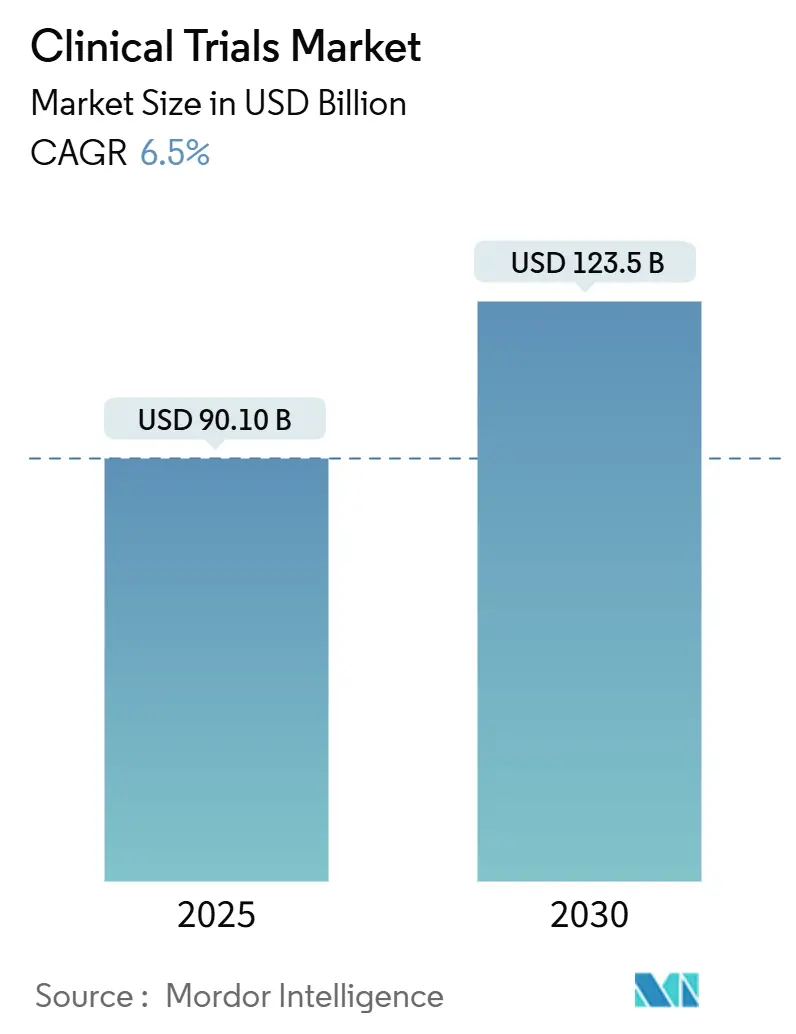
臨床試験市場は2025年に901億米ドルを創出すると推計され、2030年には1,235億米ドルに拡大し、2025年から2030年の間で6.51%のCAGRとなる見通しです。商業スポンサーは、施設関連費用を抑制し、登録タイムラインを短縮し、接続デバイスによるリアルタイム監視を支援するため、分散型またはハイブリッド実行モデルへと転換しています。2025年1月のICH E6(R3)適正臨床試験実施基準の最終採択は、リスクベース品質管理、実用的データ収集、リモートファースト監視を正式に承認することで、この転換を加速しています。腫瘍学は世界のプロトコル開始の最大シェアを維持していますが、神経学、希少疾患、細胞・遺伝子治療は、適応的デザインとバイオマーカー誘導コホート濃縮の恩恵を受けてより速く拡大しています。受託研究機関(CRO)は技術投資を通じてマージンを守る一方、新興中堅専門企業は治療の深さと地域特化の規制専門知識を提供することで大手既存企業を侵食しています。経験豊富な施設スタッフの持続的不足とバイオマーカーアッセイの複雑性増大が成長を抑制し、コストインフレーションを歴史的基準以上に保っています。
主要レポート要点
- 段階別では、後期第III相が2024年の臨床試験市場シェアの55.0%を占め、第II相は2030年まで6.8%のCAGRを示すと予測される。
- 試験デザイン別では、ランダム化比較介入試験が2024年の収益の72.3%を確保し、適応的デザインは2030年まで8.2%のCAGRで上昇する見通し。
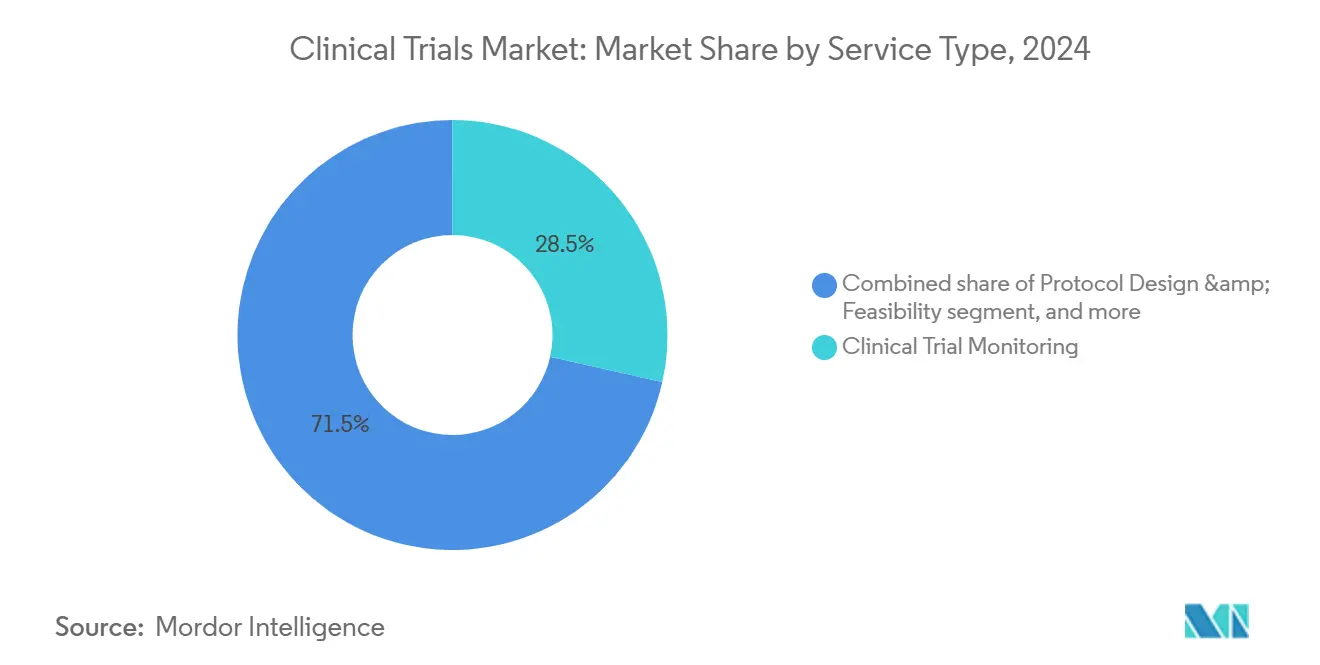
- サービス種別では、モニタリング活動が2024年の臨床試験市場規模の28.5%を占め、分散型・バーチャルサービスは14.6%のCAGRで拡大が期待される。
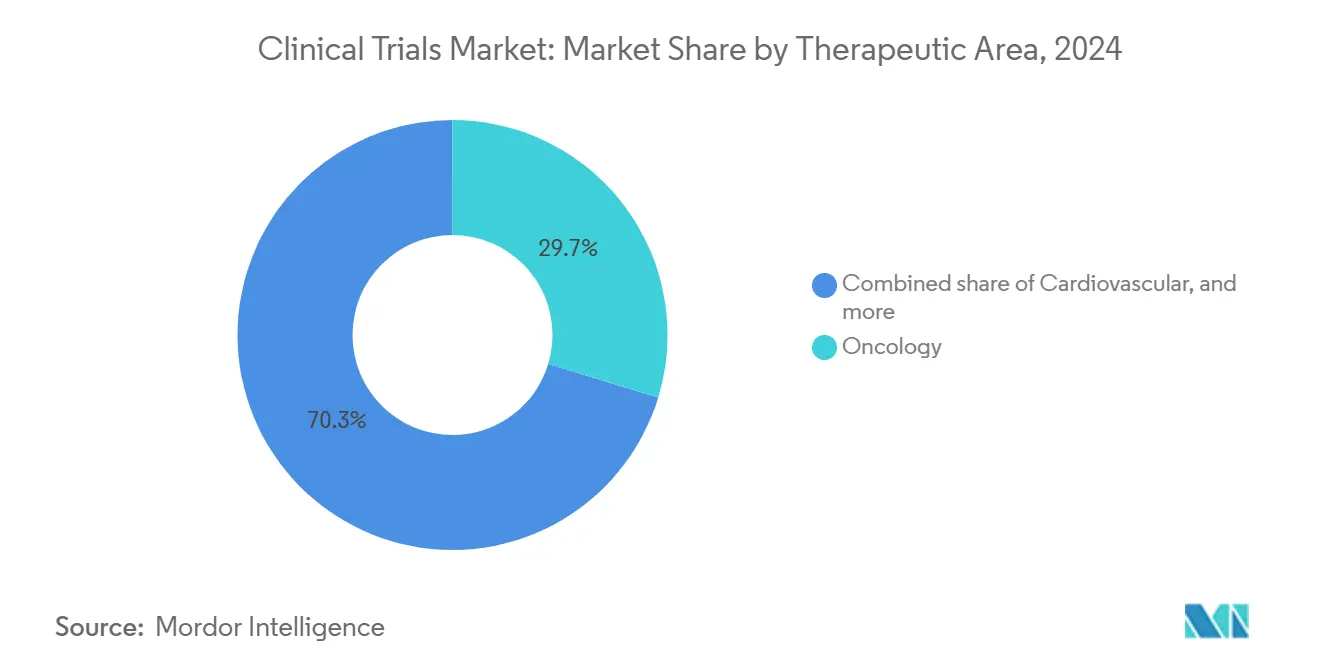
- 治療領域別では、腫瘍学が2024年の臨床試験市場規模の29.7%を占め、神経学は9.1%のCAGRで推移する見込み。
- スポンサー別では、製薬・バイオ医薬品企業が2024年に68.0%の市場シェアを維持し、政府・非営利資金調達は7.5%のCAGRで増加。
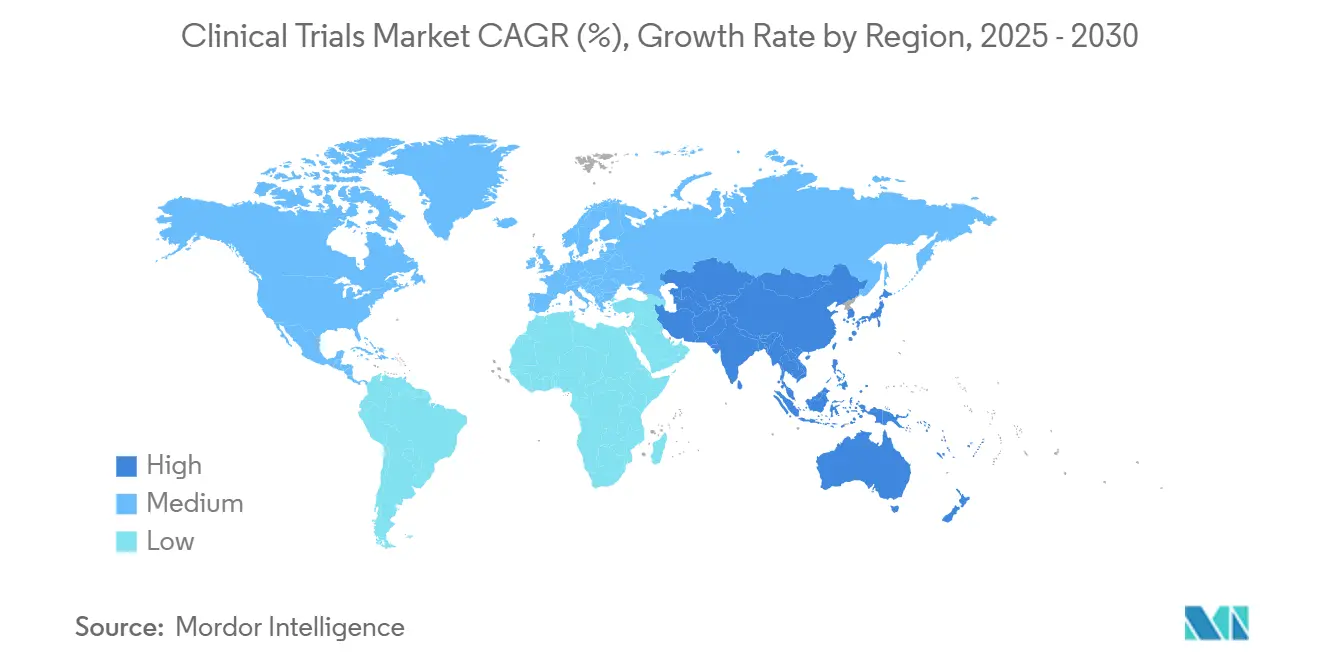
- 地域別では、北米が2024年の収益の49.2%を占め、アジア太平洋は7.9%のCAGRで最も急速に成長する地域。
世界臨床試験市場動向・洞察
ドライバーインパクト分析
| ドライバー | CAGR予測への影響(%) | 地理的関連性 | インパクトタイムライン |
|---|---|---|---|
| 分散型・ハイブリッド試験採用 | +1.9% | 世界 | 長期(4年以上) |
| 希少疾患・オーファンドラッグパイプライン拡大 | +1.6% | 北米、EU、APAC | 長期(4年以上) |
| より迅速な募集のためのアジア太平洋施設組込み | +1.4% | アジア太平洋 | 中期(2~4年) |
| AI対応患者募集ソリューション | +1.8% | 世界 | 中期(2~4年) |
| 腫瘍学試験への政府インセンティブ | +2.2% | 世界 | 長期(4年以上) |
| 承認後研究でのリアルワールドエビデンス(RWE)使用事例増加 | +1.8% | 世界 | 中期(2~4年) |
| 情報源: Mordor Intelligence | |||
分散型・ハイブリッド試験プラットフォームの加速採用
分散型アプローチでは、参加者が遠隔医療、地域ラボ、在宅デバイスを通じて来院を完了でき、移動負担を軽減し、保持率を向上させます。世界のDCT収益プールは2030年までに133億米ドルに達し、6.6%のCAGRに相当すると予測されます。患者の90%がDCT参加を受け入れ可能と考えており、リモートファースト参加への強い需要を示しています。2024年9月に発行された米国FDAの分散型臨床試験に関する最終ガイダンスは、データ完全性、インフォームドコンセント、安全性監視に関する規制要件が施設ベース試験と同等であることを確認しています[1]U.S. Food and Drug Administration, "Conducting Clinical Trials With Decentralized Elements; Guidance for Industry, Investigators, and Other Interested Parties," federalregister.gov。したがってスポンサーは、技術認定、リスクベース監視、サイバーセキュリティに関する新たな運用要件に直面しており、これらは既にベンダー選定基準を形成し、デジタルプラットフォームへのCRO投資を促進しています。
世界的な希少疾患・オーファンドラッグパイプラインの急増
ゲノミクスと次世代シーケンシングは、以前は原因不明とされていた数千の疾患の分子原因を解明し、標的治療プログラムの波を引き起こしています。約3,000万人の米国居住者が希少疾患と共に生活していますが、現在承認された治療法があるのは500疾患のみです[2]National Institutes of Health, "Rare Diseases," nih.gov。税制優遇、ユーザーフィー免除、米国希少疾病医薬品法の下での7年間独占権は、ベンチャーキャピタルと大手製薬会社の資本を惹き続けています。FDAの希少・放置疾患治療薬助成プログラムは初期ヒト試験のリスクをさらに軽減し、自然史コホート収集と分子層別化概念実証試験の高成長をもたらしています。患者集団が地理的に分散し、診断遅延が平均5~7年であるため、募集は困難であり続け、スポンサーを世界的、多施設、または完全仮想登録戦略に向かわせています。
募集タイムライン最適化のためのアジア太平洋施設組込み拡大
アジア太平洋は現在、新規臨床試験登録の半数以上を占めており、わずか5年前の3分の1から増加しています[3]Novotech, "Evolution of Clinical Trials in the Asia Pacific Region Compared to the US and EU5," novotech-cro.com。中国の規制迅速化により審査タイムラインが半減し、2017年から2021年の間にプロトコル開始が倍増した一方、インド、韓国、日本は専門的な腫瘍学・機器経路を提供しています。登録患者あたりのコストは欧米基準より30~40%低く、治療経験のない患者プールにより2~3倍速い募集が可能です。現地規制当局は共通技術文書とリスクベース監視を受け入れる傾向を強めていますが、言語、データプライバシー法、倫理委員会期待の異質性が国境を跨ぐマスタープロトコルを複雑化しています。国内・地域CROを組み合わせるハイブリッドモデルは、これらの課題を軽減し、施設カバレッジを拡張し、文化的嗜好に適合する分散型来院の利用を促進しています。
登録効率改善のためのAI対応患者募集ソリューション
機械学習アルゴリズムが電子健康記録、請求ファイル、ゲノムデータベースを調査し、潜在的適格参加者を特定し、事前スクリーニング通過率を上げ、ドロップアウトリスクを予測します。2016年以降、米国FDAはプロトコル設計またはデータ分析における人工知能に言及した約300件の提出書類を記録しています。ウェアラブルセンサーの統合によりリアルタイム安全性監視が提供され、自然言語処理により有害事象トリアージを自動化できます。アルゴリズムの透明性、データ来歴検証、バイアス軽減に重いガバナンスが必要なため、企業採用は不均一ですが、早期採用者は実行可能性・立上げにおける二桁のサイクルタイム短縮を報告しています。この技術は適応的投与アルゴリズムと合成対照群構築も支え、統計効率をさらに改善しています。
制約インパクト分析
| 制約 | CAGR予測への影響(%) | 地理的関連性 | インパクトタイムライン |
|---|---|---|---|
| 経験豊富な臨床研究コーディネーター不足 | 定量化せず | 新興市場 | 短期(2年以下) |
| バイオマーカー駆動適応的デザインの複雑性・コスト増加 | 定量化せず | 世界 | 中期(2~4年) |
| データプライバシー法(GDPR、CCPA)の精査強化によるe-同意展開阻害 | 定量化せず | 北米、EU | 中期(2~4年) |
| 西欧における研究者・施設管理費のインフレ駆動エスカレーション | 定量化せず | 西欧 | 短期(2年以下) |
| 情報源: Mordor Intelligence | |||
新興市場における経験豊富な臨床研究コーディネーターの持続的不足
アジア太平洋、中南米、東欧における急速なプロトコル成長は、ICH-GCP、リモートデータ収集、複雑な規制文書に精通した施設スタッフの供給を上回っています。完全に有能なコーディネーターを育成するには、オハイオ州立大学が提供するCAAHEP認定臨床研究修士号などの新しい臨床研究プログラムの卒業率を上回る、2~3年の指導下での経験が必要です。経験不足のチームはプロトコル逸脱リスクを高め、監視訪問を長期化し、品質保証予算を圧迫し、当初のオフショアリングを動機づけたコスト優位性の一部を侵食しています。スポンサーはベンダー契約にスタッフ訓練モジュールを組込み、移動監視ユニットを配備し、中央統計監視を強化することで対応していますが、スキルギャップは急性の短期ボトルネックのままです。
バイオマーカー駆動適応的デザインの複雑性・コスト増加
適応的濃縮、反応適応的無作為化、シームレス第II/III相フレームワークは、リアルタイム読み取りに基づいて配分を調整しますが、検証されたアッセイ、継続的データフィード、洗練されたベイズ分析に依存しています。誤分類されたバイオマーカーサンプルは、I型エラーを増大させながら試験パワーを減少させ、より大きなサンプルサイズまたはプロトコル修正を強制する可能性があります。患者あたりの直接コストは、マッチした従来のRCTより30~40%上昇し、規制当局はデザイン特徴承認前に詳細な統計運用特性シミュレーションを要求します。これらのハードルにもかかわらず、腫瘍学スポンサーは適応的手法を受け入れ続けており、連続的ゲノムおよび画像フィードバックを使用して活発な募集中にコホートを進化させるARPA-Hの2024年ADAPTプラットフォーム立上げがその証拠です。
セグメント分析
段階別:後期優勢が早期段階イノベーションを覆い隠す
第III相試験は2024年の臨床試験市場の55.0%を占めました。これは、プレミアムCRO予算を必要とする大規模多施設コホートと規制グレードエンドポイントを含むためです。単一の第III相腫瘍学プロトコルは患者あたり40,000米ドルを超える可能性があり、バイオマーカースクリーニングコストが支出増加を牽引しています。それにもかかわらず、第II相試験は適応的デザインが概念実証タイムラインを圧縮し、用量範囲設定と早期有効性を組み合わせるため、6.8%のCAGRでより速く拡大します。アジア太平洋地域は中国の迅速なIND審査経路のおかげで世界の第I相開始の58%を主催し、遺伝的に多様な集団への早期アクセスを強化しています。
スポンサーはシームレス第I/II相フレームワークを展開してgo/no-goマイルストーンを加速し、第III相投資を統制するアプローチを採用しており、これはリスクを分散し、資産優先順位付けを最適化します。ベンチャー支援バイオテック企業は、これらの試験を研究室ゲノミクス統合を持つ中堅CROに頻繁にアウトソースし、大手製薬会社は主力モダリティ向けに内部第I相ユニットを維持しています。規制機関は、統計的厳密さと柔軟性のバランスを取るガイダンスを通じてイノベーションを支援し、新規エンドポイントとデジタルバイオマーカー包含を奨励しています。これらの動向が組み合わさり、臨床試験市場において後期段階試験が支出の大部分を吸収し続ける一方で、探索段階がよりデータリッチになるパイプラインを強化しています。
臨床試験市場:段階別市場シェア
| 第III相 | 55.0% |
|---|---|
| 第I相他の合計シェア | 45.0 |
| 情報源: Mordor Intelligence | |
試験デザイン別:適応的アプローチが勢い拡大
介入ランダム化比較試験は規制ゴールドスタンダードのままであり、2024年の収益の72.3%を吸収し、ほとんどの治療薬のリスク計算を支えています。ICH E6(R3)ガイダンスは比例的監視を明示的に承認し、スポンサーが中間解析と事前指定停止ルールを組み込むことを奨励し、それにより適応的フレームワークの8.2% CAGRを牽引しています。腫瘍学が最前線にあります:アンブレラ、バスケット、プラットフォーム構造は、共有対照群を活用して登録負担を削減しながら、複数のバイオマーカー定義コホートを並行してテストします。
臨床試験市場は、異質性が治療評価を複雑化する感染症、神経疾患、自己免疫疾患のプラットフォーム試験を次第に統合しています。シミュレーション運用特性パッケージは、エラー率制御を実証するために規制提出書類に添付され、中央統計監視は従来の現地検証よりも迅速にデータ異常をフラグ立てします。マスタープロトコル構成体の継続的受容は適応的濃縮の使用を広げ、柔軟なデザインがもはや実験的ではなく、臨床試験市場内の現代的エビデンス生成の本質的特徴であるという認識を強化しています。
サービス種別:モニタリングが支配的、バーチャルサービスが急増
モニタリングは、スポンサーが複雑な分子アッセイと高コストエンドポイントの時代においてプロトコル遵守、データ清浄性、参加者保護を優先したため、2024年収益の28.5%を占めました。ICH E6(R3)が義務付けるリスクベース品質管理システムは、徹底的なソースデータ検証から重要変数に焦点を当てた中央分析へと予算をシフトします。それでも、複雑な介入で注入薬局チェックや画像較正を必要とする場合、現地監視は不可欠です。
バーチャルサービスラインは最も急成長のコンポーネントであり、リモートデバイス、電子インフォームドコンセント、遠隔来院の拡大に伴い14.6%のCAGRを記録しています。分散型運用モデルは地理的障壁を削減し、人口統計的包含性を広げ、米国FDAの2023年代表性不足集団登録強化に関する草案ガイダンスなど、規制当局が設定する多様性義務を満たします。アジア太平洋の病院は、バーチャル評価を組み込むために技術ベンダーとのパートナーシップを増やしており、スポンサーに低コスト施設と高技術データ取得を融合した生態系を提供しています。その結果、臨床試験市場はデータ中心、患者中心のサービスバンドルを通じて価値を再定義しています。
治療領域別:神経学成長中の腫瘍学リーダーシップ
腫瘍学は2024年支出の29.7%を牽引しました。これは、高いアンメットニーズ、イノベーションに対する支払者の受容性、バイオマーカーの複雑性がプロトコル投資を押し上げるためです。業界資金によるがん試験は連邦政府支援研究を8対1で上回り、市場投入スピードが数十億ドル規模のフランチャイズ予測を変える可能性がある環境を創出しています。神経学は、アミロイドおよびタウイメージングの突破口と希少神経変性疾患に対する遺伝子沈黙戦略に推進され、2030年まで9.1%のCAGRで全領域を上回ります。
希少疾患プログラムは腫瘍学と神経学の両方を横断し、適応的デザインを活用して超小規模コホートと自然史比較対照を管理しています。AI駆動セグメンテーションツールは疾患進行を予測し、エンドポイント期間を調整し、サンプルサイズを膨らませることなく統計パワーを改善します。細胞ベースおよび遺伝子編集介入の台頭はさらなる複雑性を加え、スポンサーにアッセイ検証と長期安全性監視の強化を促しています。こうした要因が、臨床試験市場内で高生物学リスク・高リターンポートフォリオへの継続的資本再配分を支えています。
スポンサー種別:製薬企業がリード、政府資金調達が成長
製薬・バイオ医薬品企業は2024年の総価値の68%を占め、直接施設支払いに300億米ドル以上を投じ、米国経済活動で620億米ドルを創出しました。業界支援は2018年以降発表された最も引用数の多い査読試験の半数以上も資金提供し、研究課題とデザイン選択に対する支配的影響力を示しています。
政府、学術、非営利団体は7.5%のCAGRで参加を拡大し、抗菌薬耐性、パンデミック準備、希少小児疾患など公衆衛生優先事項をターゲットにします。官民パートナーシップは基礎科学洞察と商業開発力を融合し、mRNAワクチンやCRISPR治療薬などフロンティアモダリティのリスクを軽減します。資金調達多様化は臨床試験市場に回復力を加え、セクター特有のショックから保護しつつ、透明性期待とデータ共有義務も高めています。
地域分析
北米は2024年の世界収益の49.2%を創出し、成熟した規制生態系、先進研究者ネットワーク、豊富な科学資本に支えられました。州レベル経済乗数は試験支出の地域価値を強調します:フロリダが83億米ドル、テキサスが77億米ドル、カリフォルニアが71億米ドルの2024年活動を捕捉しました。地域当局は単純な量より方法論的イノベーションを次第に優先しており、分散型試験、適応的デザイン、リアルワールドエビデンス統合に関する機関ガイダンスがその証拠です。ここでの臨床試験市場はコスト圧力に直面しており、戦略的米国ハブを維持しながら低強度手順をオフショアするハイブリッドモデルにスポンサーを向かわせています。
アジア太平洋は7.9%のCAGRで成長すると予測され、規制自由化、審査タイムライン加速、大規模治療経験なし集団を通じて世界臨床試験市場を再形成しています。中国とインドを合わせると総活発プロトコルのほぼ40%を占めます。韓国の中央IRBフレームワーク、日本の再生医療条件付承認経路、台湾のブロックチェーンベースe-source検証用データ完全性サンドボックスは、総合的に差別化されたニッチを確立しています。この地域のコスト構造(患者あたり30~40%安価)と募集速度(欧米基準の2~3倍速)は説得力のある提案を創出します。しかし、データプライバシー法と英語熟練度の変動は国境跨ぎマスタープロトコル課題をもたらし、地域ノウハウと世界プロセス標準化を融合するCRO提携を促しています。
欧州は相当な科学専門知識と専門インフラを保持していますが、長期化したスタートアップタイムラインとコストインフレーションの中で、臨床試験市場における相対的シェアは下方に傾いています。臨床試験規則(CTR)は中央ポータルを通じて多加盟国許可の合理化を目指し、欧州医薬品庁は患者焦点アウトカム測定を強調しています[4]European Medicines Agency, "Clinical trial," ema.europa.eu。Brexitは追加の複雑層を導入します:英国スポンサーは二重コンプライアンストラックをナビゲートしなければなりませんが、新しいウィンザー・フレームワークは北アイルランドのデータフローを促進します。将来の成長は、欧州の学術ネットワークが競争力を保持する希少疾患、先進治療薬、複雑統計手法に集中する可能性が高いです。
競争環境
臨床試験市場は中程度の集中度を示しています:最大5社のCRO-IQVIA、Labcorp、ICON、Parexel、Syneos-は2024年に収益の約40%を合計で保有しました。IQVIAは世界データサイエンスプラットフォームを活用し、75ヶ国30適応症で500以上の分散型またはハイブリッド試験を実施し、技術スタックのGDPRコンプライアンス検証を達成しています。Labcorpは2023年に臨床開発部門のスピンオフを完了し、研究所・中央検査サービスへの戦略焦点を鋭化させ、新独立体はCRO拡大を追求しています。ICONのPRA Health Sciences120億米ドル買収は治療・地理フットプリントを統合し、ICONを世界第3位のCROに押し上げました。
中堅CROは治療専門化(細胞治療、眼科学、デジタルヘルス統合など)を利用し、特注専門知識を求めるスポンサーからプロトコルを獲得します。中国、インド、東南アジアの地域CROは多国籍企業とパートナーして、現地倫理承認、言語ローカライゼーション、市販後監視要件をナビゲートします。電子同意ベンダー、データ集約プラットフォーム、ウェアラブル製造業者との技術パートナーシップが入札を差別化し、リスクベース品質管理を支援します。競争は予測登録モデルを提供し、施設選定時間を削減するベンダーを含むAI対応実行可能性周辺でも激化します。
ホワイトスペース機会は希少疾患、複雑生物製剤、分散型サービス提供に集中しています。スポンサーは、コンプライアンス品質フレームワーク下でリモート患者アクセス、在宅採血、機器テレメトリを統合できるベンダーを評価します。CROは患者データ保護のためにサイバーセキュリティ能力に積極投資しており、特に欧州でGDPR罰金が世界売上高の4%を超える地域、および2025年超党派提案が国家プライバシー基準の調和を目指す米国でそうです。これらのダイナミクスは、臨床試験市場内の競争優位性が規模のみではなく、技術成熟度、治療焦点、規制流暢性に次第に依存することを確保します。
臨床試験業界リーダー
-
IQVIA Holdings Inc.
-
Laboratory Corporation of America (Labcorp)
-
ICON plc
-
Parexel International Corp.
-
Syneos Health
- *免責事項:主要選手の並び順不同
最近の業界動向
- 2025年2月:ICON plcがICH E6(R3)の詳細分析を発表し、リアルタイムリスク評価における技術の役割を強調。
- 2025年1月:ICHがE6(R3)主要ガイドラインを最終化し、27年間で初のGCP全面見直しを開始。
- 2024年12月:FDAがE6(R3)附属書2草案ガイダンスを発行し、分散型・実用的デザイン原則を強化。
- 2024年11月:FDAが分散型試験に関するガイダンスを最終化し、リモートデータ完全性・参加者安全性期待を明確化。
- 2024年11月:ICHがE6(R3)適正臨床試験実施基準附属書2最終版を発表し、リスクベース品質管理の実施ガイダンスを詳述。
- 2024年9月:FDAが多地域腫瘍学試験に関する草案ガイダンスを発表し、米国登録割合の減少に対処。
- 2024年3月:ARPA-Hが、細分化患者データに基づく進化的腫瘍学試験デザインの先駆けとなるADAPTプログラムを開始。
世界臨床試験市場レポート範囲
レポート範囲に従い、臨床試験は臨床研究下で実施され、規制されたプロトコルに従う実験です。これらの試験は主として新開発薬物の安全性・有効性に関するデータ取得のために実行されます。臨床試験データは薬事承認と市場導入に必須です。このプロセスは高額で時間を要し、全段階で専門知識を必要とします。
臨床試験セクターは段階、デザイン、地域別にセグメント化されています。段階別では、市場は第I相、第II相、第III相、第IV相にセグメント化されます。デザイン別では、市場は治療研究と観察研究にセグメント化されます。地域別では、市場は北米、欧州、アジア太平洋、中東・アフリカ、南米にセグメント化されます。レポートpdfは世界主要地域17ヶ国の推定市場規模・動向もカバーします。市場レポートpdfは上記全セグメントの価値(米ドル)を提供します。
| 第I相 |
| 第II相 |
| 第III相 |
| 第IV相 |
| 介入・治療研究 |
| 観察研究 |
| 拡大アクセス研究 |
| プロトコル設計・実行可能性 |
| 施設特定・立上げ |
| 規制申請・承認 |
| 臨床試験モニタリング |
| データ管理・生物統計 |
| メディカルライティング |
| その他サービス種別 |
| 腫瘍学 |
| 心血管 |
| 神経学 |
| 感染症 |
| 代謝疾患(糖尿病、肥満) |
| 免疫学・自己免疫 |
| その他治療領域 |
| 製薬・バイオ医薬品企業 |
| 医療機器企業 |
| 学術・研究機関 |
| 政府・非営利組織 |
| 北米 | 米国 |
| カナダ | |
| メキシコ | |
| 欧州 | ドイツ |
| 英国 | |
| フランス | |
| イタリア | |
| スペイン | |
| その他欧州 | |
| アジア太平洋 | 中国 |
| 日本 | |
| インド | |
| 韓国 | |
| オーストラリア | |
| その他アジア太平洋 | |
| 中東・アフリカ | GCC |
| 南アフリカ | |
| その他中東・アフリカ | |
| 南米 | ブラジル |
| アルゼンチン | |
| その他南米 |
| 段階別 | 第I相 | |
| 第II相 | ||
| 第III相 | ||
| 第IV相 | ||
| 試験デザイン別 | 介入・治療研究 | |
| 観察研究 | ||
| 拡大アクセス研究 | ||
| サービス種別 | プロトコル設計・実行可能性 | |
| 施設特定・立上げ | ||
| 規制申請・承認 | ||
| 臨床試験モニタリング | ||
| データ管理・生物統計 | ||
| メディカルライティング | ||
| その他サービス種別 | ||
| 治療領域別 | 腫瘍学 | |
| 心血管 | ||
| 神経学 | ||
| 感染症 | ||
| 代謝疾患(糖尿病、肥満) | ||
| 免疫学・自己免疫 | ||
| その他治療領域 | ||
| スポンサー種別 | 製薬・バイオ医薬品企業 | |
| 医療機器企業 | ||
| 学術・研究機関 | ||
| 政府・非営利組織 | ||
| 地域 | 北米 | 米国 |
| カナダ | ||
| メキシコ | ||
| 欧州 | ドイツ | |
| 英国 | ||
| フランス | ||
| イタリア | ||
| スペイン | ||
| その他欧州 | ||
| アジア太平洋 | 中国 | |
| 日本 | ||
| インド | ||
| 韓国 | ||
| オーストラリア | ||
| その他アジア太平洋 | ||
| 中東・アフリカ | GCC | |
| 南アフリカ | ||
| その他中東・アフリカ | ||
| 南米 | ブラジル | |
| アルゼンチン | ||
| その他南米 | ||
レポートで回答される主要質問
ABC現在の臨床試験市場価値とその成長速度は?
臨床試験市場は2025年に901億米ドルを創出すると推計され、2030年までに1,235億米ドルに達し、6.5%のCAGRを反映すると予測されます。
どの試験段階が最高支出を惹きつけますか?
第III相は患者あたり高コストを牽引する大規模多地域コホートと規制グレードエンドポイントを含むため、総支出の55%を占めています。
分散型臨床試験がスポンサーにとって重要な理由は?
分散型またはハイブリッドデザインは患者移動を削減し、保持率を改善し、リアルタイムリモート監視を可能にし、より迅速な募集と潜在的に短いタイムラインを支援します。
アジア太平洋が臨床開発にとって魅力的な理由は?
アジア太平洋の試験は、大規模治療経験なし集団と合理化された規制フレームワークにより、患者あたり30~40%安く、欧米地域より2~3倍速い募集が可能です。
希少疾患研究の機会規模は?
7,000の特定された希少疾患に対して500の承認治療のみであるため、希少疾患プログラムは税額控除と市場独占インセンティブに後押しされた相当な成長分野を代表します。
今日の市場における主要CROは誰ですか?
IQVIAとLabcorpがリードし、ICON、Parexel、Syneosが続きます;これらは合わせて世界CRO収益の約40%を保有しています。
最終更新日:


