Tendances du marché de Traitement du syndrome myélodysplasique (SMD) Industrie
Le segment des greffes de cellules souches devrait détenir une part de marché importante sur le marché du traitement du syndrome myélodysplasique (SMD).
Pour les patients atteints de syndromes myélodysplasiques, la transplantation de cellules souches (SCT) offre une thérapie potentiellement bénéfique. Il existe deux principaux types de SCT, lune est une greffe allogénique de cellules souches et lautre est une greffe autologue de cellules souches. Lors d'une greffe allogénique de cellules souches, après la destruction de la moelle osseuse, le patient reçoit des cellules souches hématopoïétiques d'une autre personne, le donneur. Il sagit du type de greffe le plus courant pour le SMD. Par exemple, l'étude intitulée La transplantation allogénique de cellules souches peut surmonter l'impact négatif de la myélofibrose sur le pronostic du syndrome myélodysplasique publiée sur PubMed.gov en août 2021, a conclu que les patients atteints de myélofibrose (MF) -2/3 avaient un pronostic plus sombre. que ceux atteints de myélofibrose (MF) -0/1 chez les patients sans greffe allogénique de cellules souches hématopoïétiques (allo-HSCT)
Cependant, les SCT allogéniques peuvent avoir des effets secondaires graves, voire potentiellement mortels ; ainsi, ils sont généralement pratiqués sur des patients plus jeunes et en meilleure santé. Des patients dans la soixantaine et même dans la soixantaine ont subi une greffe avec succès, mais la SCT est généralement réalisée avec une chimiothérapie et/ou une radiothérapie moins intensive (intensité réduite) chez les patients plus âgés. Des doses plus faibles ne tuent peut-être pas toutes les cellules de la moelle osseuse, mais elles suffisent juste à permettre aux cellules du donneur de prendre racine et de se développer dans la moelle. Les doses plus faibles entraînent également moins deffets secondaires, ce qui rend ce type de greffe plus tolérable pour les patients plus âgés. Néanmoins, certains effets secondaires graves restent possibles
De plus, les patients reçoivent leurs propres cellules souches après une greffe de cellules souches autologues (qui ont été retirées avant le traitement). Comme la moelle osseuse du patient contient des cellules souches anormales, ce type de greffe est rarement utilisé chez les patients atteints de SMD
Ainsi, les facteurs mentionnés ci-dessus devraient avoir un impact sur la croissance du segment au cours de la période d'analyse
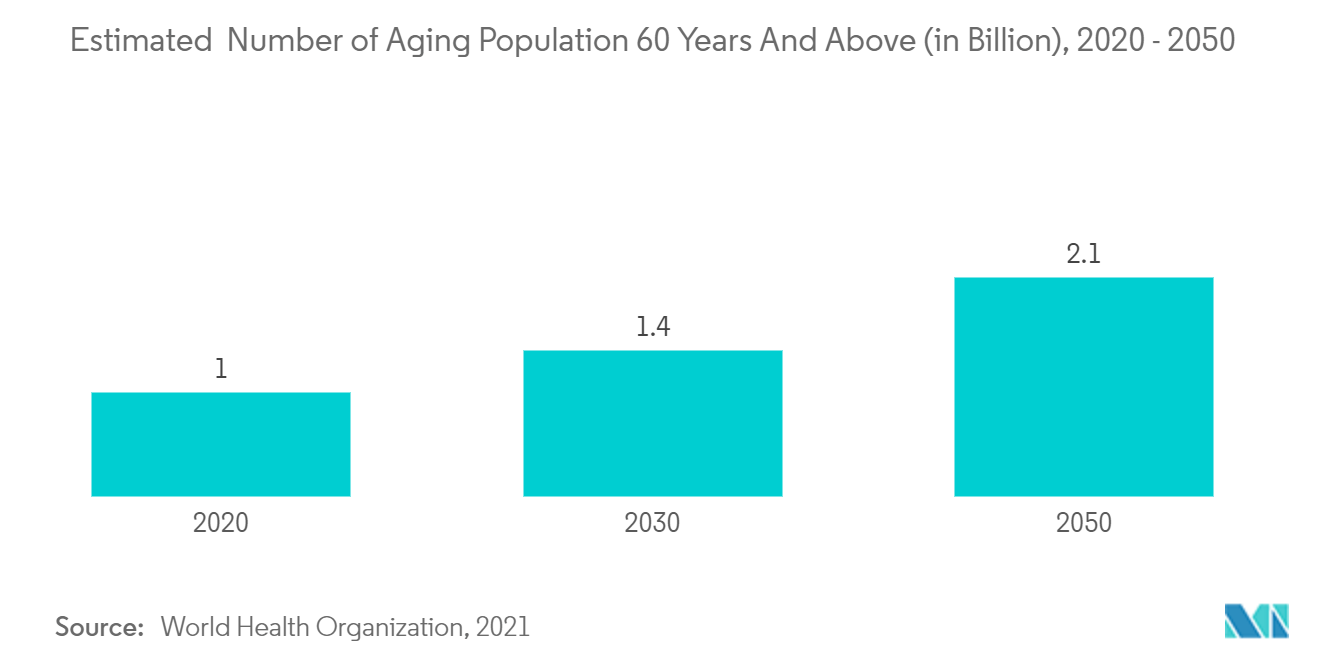
LAmérique du Nord devrait détenir une part importante du marché et devrait faire de même au cours de la période de prévision.
LAmérique du Nord domine le marché mondial du traitement du syndrome myélodysplasique (SMD) en raison de laugmentation de la prévalence du syndrome myélodysplasique, de ladoption précoce de nouveaux traitements, des investissements élevés en RD dans le développement de nouveaux médicaments et de la présence dinfrastructures de santé sophistiquées. Selon lAmerican Society of Clinical Oncology (ASCO) 2022, le SMD touche environ 10 000 personnes aux États-Unis chaque année. Le SMD est rare chez les personnes de moins de 50 ans. Cependant, les personnes dans la soixantaine sont les plus susceptibles den développer. Le nombre de personnes diagnostiquées chaque année avec un SMD devrait augmenter à mesure que la population des États-Unis vieillit
De plus, les approbations de produits augmentent à un rythme rapide, ce qui contribue à stimuler la croissance du marché. Takeda Pharmaceutical Company Limited, par exemple, a annoncé en juillet 2020 que la FDA avait accordé la désignation de thérapie révolutionnaire à son médicament expérimental, le pevonedistat, pour le traitement des patients atteints de syndromes myélodysplasiques à haut risque (HR-MDS). Le pevonedistat, un inhibiteur de l'enzyme activatrice NEDD8 (NAE) premier de sa classe, pourrait être le premier nouveau traitement pour les patients HR-MDS depuis plus d'une décennie, élargissant les options de traitement auparavant limitées à la monothérapie HMA. Même avec les options de traitement actuelles, les personnes atteintes de HR-MDS continuent davoir de mauvais résultats. De même, Novartis a annoncé en novembre 2021 que la Food and Drug Administration (FDA) des États-Unis avait accordé une désignation accélérée au sabatolimab (MBG453) utilisé dans le traitement des patients adultes atteints de syndromes myélodysplasiques (SMD) définis par une catégorie de risque IPSS-R. à risque élevé ou très élevé en association avec des agents hypométhylants. De même, en septembre 2020, Gilead Sciences, Inc. a annoncé que la Food and Drug Administration (FDA) des États-Unis avait accordé au magrolimab, un anticorps monoclonal anti-CD47 expérimental premier de sa classe, pour le traitement du syndrome myélodysplasique nouvellement diagnostiqué, un Désignation de thérapie révolutionnaire
En outre, la sensibilisation croissante des patients aux États-Unis devrait stimuler la croissance du marché au cours de la période de prévision. Par exemple, en septembre 2020, Jazz Pharmaceuticals plc a annoncé le lancement de Find the Right Fit, un programme d'éducation des patients aux États-Unis développé en collaboration avec la Myelodysplastic Syndromes (MDS) Foundation, Inc. et la Cancer Support Community pour donner aux personnes atteintes de leucémie myéloïde aiguë secondaire (sAML) et SMD
Ensemble, ces facteurs sont susceptibles de soutenir la croissance du marché du traitement du syndrome myélodysplasique (SMD) dans la région nord-américaine