Tendances du marché de Externalisation des affaires réglementaires mondiales dans le domaine de la santé Industrie
Le segment de lenregistrement des produits et des applications dessais cliniques devrait détenir une part de marché importante au cours de la période de prévision
Lenregistrement dun produit fait référence à la demande dapprobation réglementaire accordée par lautorité compétente dans un pays ou un territoire donné pour permettre la commercialisation, la distribution, la vente ou limportation dun produit dans le pays ou la région. La demande dessai clinique fait référence à la soumission aux autorités réglementaires nationales compétentes pour obtenir lautorisation de mener un essai clinique dans le pays. La demande dessai clinique contient des informations détaillées sur le médicament expérimental et lessai prévu, permettant aux autorités réglementaires dévaluer la faisabilité de létude
Laugmentation de lexternalisation des demandes dessais cliniques et des enregistrements de produits dans les pays développés et en développement stimule le segment de lenregistrement des produits et des applications dessais cliniques au cours de la période de prévision. En raison de la complexité du processus denregistrement des produits, du manque de professionnels dans lindustrie et du manque de capacités internes, la plupart des entreprises pharmaceutiques et de dispositifs médicaux sous-traitent leurs activités denregistrement des produits à des fournisseurs de services tiers. En outre, les changements constants et la mise à jour des affaires réglementaires stimulent également lexternalisation de ces services. Par exemple, le 31 janvier 2022, lAgence européenne des médicaments a annoncé lharmonisation réglementaire des essais cliniques dans lUE. Il a également lancé un nouveau système dinformation sur les essais cliniques (SIEC). Cela devrait propulser la croissance du segment au cours de la période de prévision
Ainsi, tous les facteurs mentionnés ci-dessus devraient stimuler la croissance du segment au cours de la période de prévision
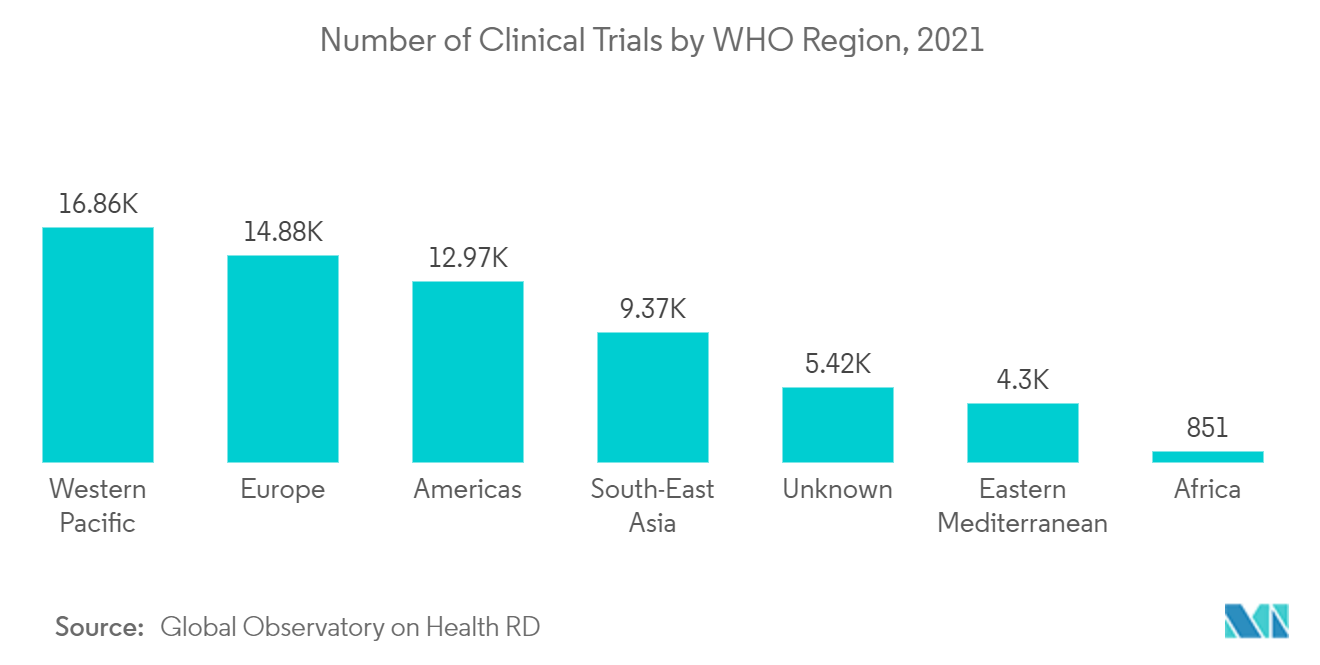
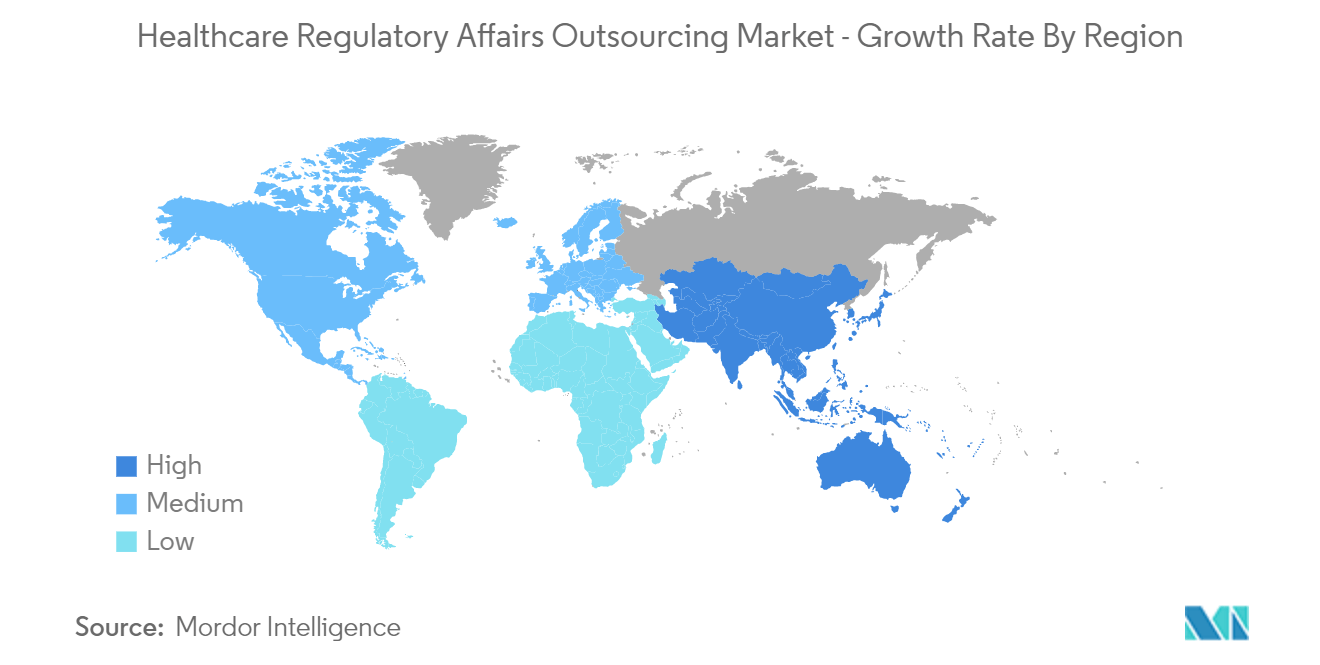
LAmérique du Nord devrait détenir une part de marché importante au cours de la période de prévision
La pression sur les prix due à lévolution du scénario de remboursement et à la concurrence des génériques pousse les grandes sociétés pharmaceutiques à externaliser les activités daffaires réglementaires qui devraient stimuler la croissance des services dexternalisation de la réglementation des soins de santé en Amérique du Nord. De plus, lactivité croissante de recherche et développement et laugmentation des essais cliniques devraient stimuler la croissance du marché régional. Par exemple, selon lObservatoire mondial de la RD en santé, les États-Unis ont enregistré 10 870 essais cliniques en 2021, soit 18,1 % du total. Selon la même source, le Canada a enregistré 2 099 essais cliniques en 2021, soit 3,5 % du total. Ainsi, de nombreux essais cliniques dans la région sont susceptibles de stimuler le marché de lexternalisation des affaires réglementaires
De plus, la présence dacteurs régionaux clés et les collaborations stratégiques dans lindustrie stimulent la croissance du marché. Par exemple, en avril 2021, Parexel et Veeva Systems ont annoncé un partenariat stratégique pour accélérer les essais cliniques en tirant parti de linnovation technologique et des processus. Les deux entreprises bénéficieront des services de conseil en réglementation de lautre
Ainsi, tous les facteurs ci-dessus devraient stimuler la croissance du marché dans la région Amérique du Nord au cours de la période de prévision
Externalisation des affaires réglementaires mondiales dans le domaine de la santé Instantanés du rapport
- Externalisation des affaires réglementaires mondiales dans le domaine de la santé Taille du Marché
- Externalisation des affaires réglementaires mondiales dans le domaine de la santé Part de marché
- Externalisation des affaires réglementaires mondiales dans le domaine de la santé Tendances du marché
- Externalisation des affaires réglementaires mondiales dans le domaine de la santé entreprises

