Tendances du marché de Traitement de la dystrophie musculaire de Duchenne Industrie
Le segment du saut dexon devrait détenir une part de marché importante au cours de la période de prévision
Les délétions internes du gène de la dystrophine, une protéine essentielle à la préservation de l'intégrité des membranes des cellules musculaires, sont la principale cause de la dystrophie musculaire de Duchenne. Une stratégie thérapeutique prospective consiste à masquer un exon à proximité de lendroit où les autres sont absents pour permettre aux exons restants de se rassembler. Le saut dexon est lune des stratégies thérapeutiques les plus efficaces pour restaurer lexpression dune protéine dystrophine raccourcie mais fonctionnelle
De plus, les acteurs du marché se concentrent sur les lancements fréquents de technologies de saut dexon, qui constituent un facteur important pour le segment, propulsant ainsi la croissance du marché. Par exemple, en juin 2022, Novartis a annoncé que la Commission européenne (CE) avait approuvé Tabrecta (capmatinib) comme monothérapie pour le traitement des adultes atteints d'un cancer du poumon non à petites cellules (CPNPC) avancé présentant des mutations provoquant l'exon 14 (METex14). sauter et qui ont besoin d'un traitement systémique après avoir reçu une immunothérapie et/ou une chimiothérapie à base de platine. De même, en février 2021, Sarepta Therapeutics, Inc. a annoncé que la Food and Drug Administration (FDA) des États-Unis avait approuvé AMONDYS 45 (casimersen). AMONDYS 45 est un oligonucléotide antisens de la plateforme d'oligomères phosphorodiamidate morpholino (PMO) de Sarepta, indiqué pour le traitement de la dystrophie musculaire de Duchenne (DMD) chez les patients présentant une mutation confirmée susceptible de sauter l'exon 45
Par conséquent, en raison des lancements de produits et des progrès technologiques, une croissance considérable du segment est attendue au cours de la période de prévision
La région Amérique du Nord devrait connaître une croissance considérable au cours de la période de prévision
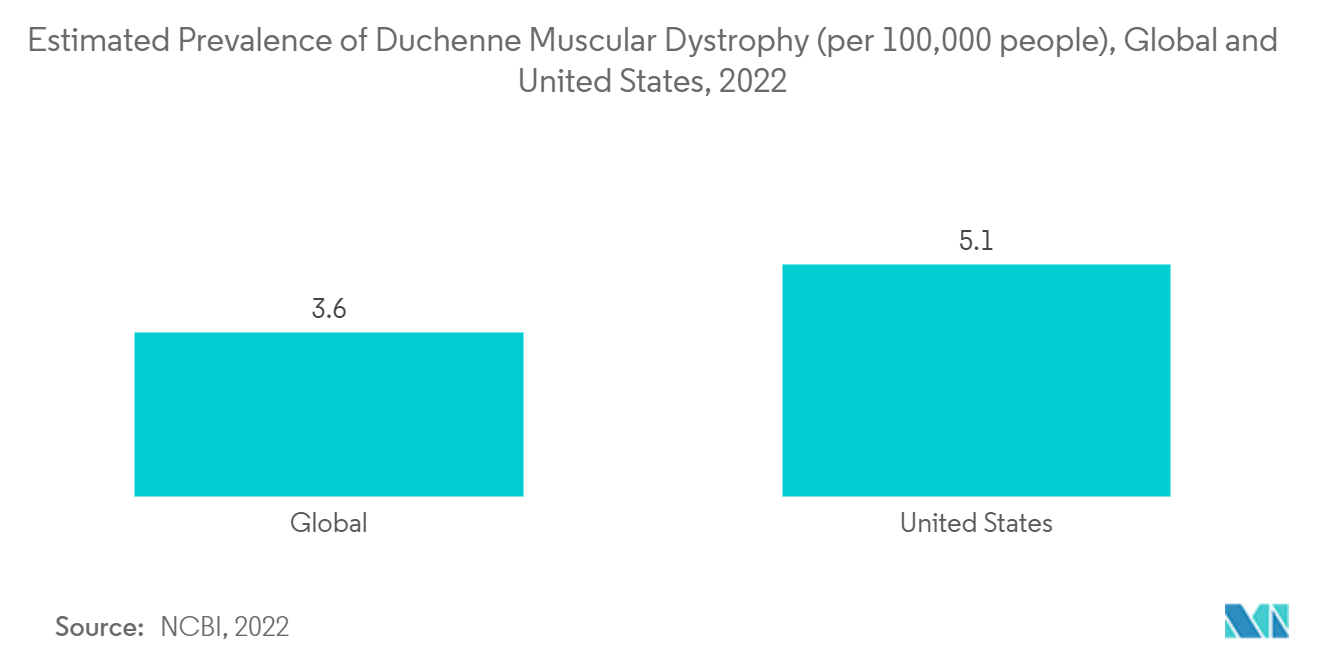
La région nord-américaine devrait connaître une croissance considérable en raison des innovations en matière de nouveaux produits, des dépenses de santé élevées et des programmes de sensibilisation du gouvernement. En raison de la prévalence accrue de la maladie et des lancements anticipés de candidats attractifs, les États-Unis ont dominé le marché régional et devraient conserver cette position. De plus, le marché devrait se développer à mesure que davantage dessais cliniques sont menés à léchelle mondiale, en particulier aux États-Unis. Par exemple, lElamipretide a reçu la désignation de médicament orphelin du bureau de développement des produits orphelins de la Food and Drug Administration (FDA) des États-Unis en mai 2022 pour traiter les patients atteints de dystrophie masculaire de Duchenne (DMD). De même, en février 2021, la FDA a approuvé l'Amondys 45 (casimersen injectable) de Sarepta Therapeutics, un oligonucléotide antisens, pour le traitement des personnes atteintes de dystrophie musculaire de Duchenne. De plus, l'injection de Viltepso (viltolarsen) a reçu une autorisation accélérée de la Food and Drug Administration des États-Unis en août 2020 pour le traitement de la dystrophie musculaire de Duchenne (DMD) chez les patients présentant une mutation vérifiée du gène DMD susceptible de sauter l'exon 53. Ainsi, ces facteurs devraient propulser la croissance du marché dans la région nord-américaine
Le marché du traitement de la dystrophie musculaire de Duchenne devrait connaître une croissance significative aux États-Unis en raison des énormes besoins non satisfaits et des initiatives favorables des principaux acteurs. Par exemple, en avril 2022, Pfizer Inc. a annoncé son intention douvrir les premiers sites aux États-Unis dans le cadre de létude de phase 3 évaluant la thérapie génique expérimentale à base de mini-dystrophine, le fordadistrogene movaparvovec, chez des patients ambulatoires atteints de dystrophie musculaire de Duchenne (DMD). En outre, selon les estimations du marché pour la maladie DMD, les médicaments en cours de développement devraient conquérir le marché dans les années à venir, ce qui entraînerait un triplement de la part de marché des thérapies à saut d'exon et une diminution de moitié de la part de marché des stéroïdes. Huit nouveaux médicaments en préparation, le prix élevé des thérapies géniques et cellulaires et laugmentation prévue des taux de traitement seront tous des moteurs de croissance importants pour le marché de la DMD. Ainsi, une croissance significative de la croissance du marché est attendue au cours de la période de prévision aux États-Unis