Tendencias del Mercado de Pruebas analíticas farmacéuticas Industria
Se espera que el segmento de pruebas de estabilidad muestre un crecimiento significativo del mercado durante el período de pronóstico
Las pruebas de estabilidad se realizan para evaluar la capacidad del fármaco para conservar sus propiedades durante toda su vida útil. Los estudios de estabilidad de productos farmacéuticos o fármacos son uno de los parámetros más importantes para el desarrollo de nuevos fármacos y nuevas formulaciones. Las pruebas de estabilidad se realizan en base a cinco parámetros químico, físico, microbiológico, terapéutico y de toxicidad. La degradación con respecto a cualquiera de estos parámetros puede conllevar riesgos para la salud.
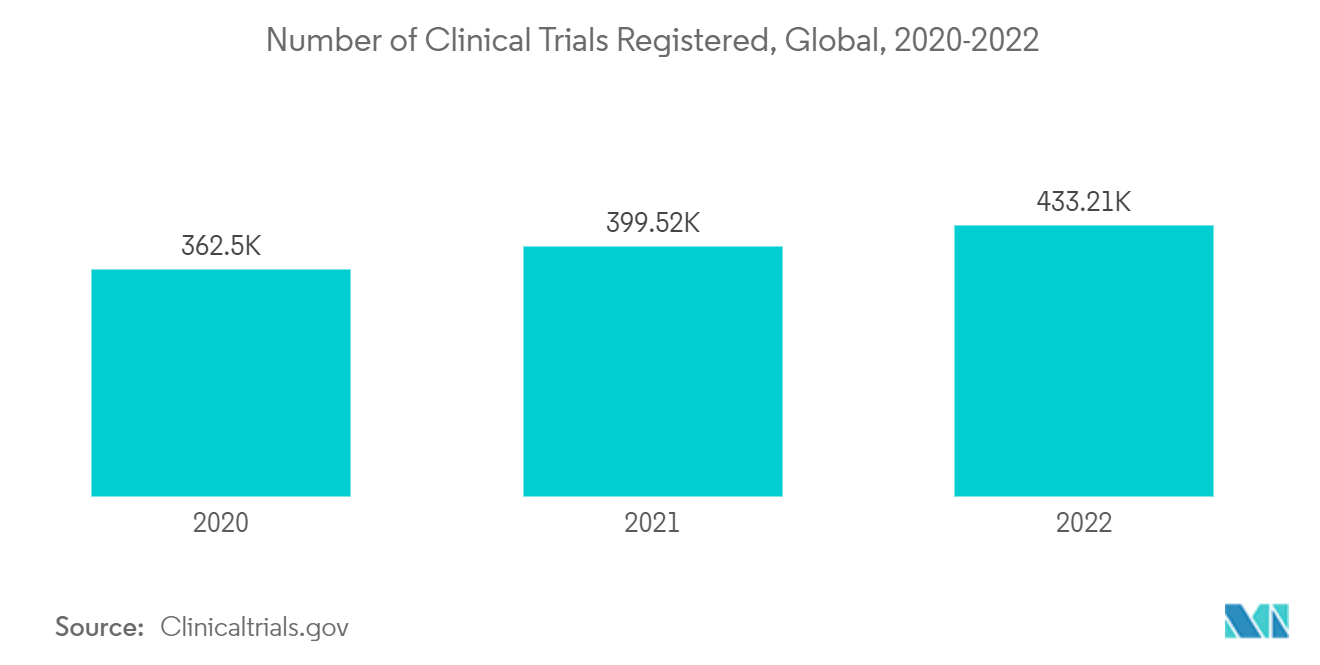
La predicción de la vida útil es vital para el desarrollo de productos farmacéuticos en todas sus formas farmacéuticas. También se utiliza para determinar las condiciones de almacenamiento y sugerir instrucciones en la etiqueta. Las pruebas de estabilidad de productos farmacéuticos garantizan el mantenimiento de la calidad, seguridad y eficacia del producto durante toda su vida útil, lo que se considera un requisito previo para la aceptación y aprobación de cualquier producto farmacéutico. Y estos estudios deben seguir las directrices de la Organización Mundial de la Salud. Según la actualización de Clinicaltrial.gov 2022, hasta el año en curso se han registrado 433,207 estudios, de los cuales el 53% están registrados fuera de los Estados Unidos y el 31% están registrados en los Estados Unidos. Por lo tanto, se espera que estos factores impulsen el crecimiento del segmento
Las iniciativas estratégicas adoptadas por los actores clave, como lanzamientos de productos, aprobaciones y asociaciones, también están impulsando el crecimiento del segmento. Por ejemplo, en julio de 2021, LGM Pharma lanzó sus servicios de estabilidad y pruebas analíticas para desarrolladores y fabricantes de productos farmacéuticos, incluidas farmacias de compuestos. Se estima que estos desarrollos impulsarán el crecimiento del segmento durante el período de pronóstico
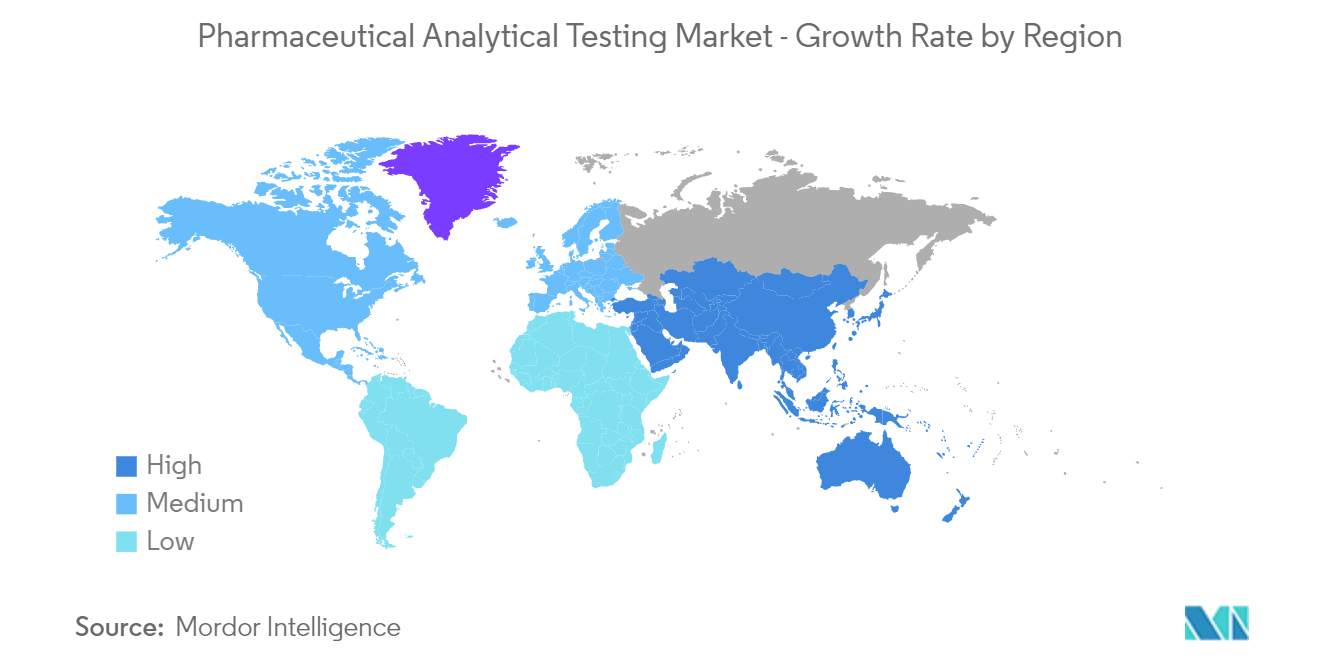
América del Norte tiene una participación significativa en el mercado y se espera que haga lo mismo durante el período de pronóstico
Se espera que América del Norte sea una región dominante en el mercado de pruebas analíticas farmacéuticas debido al creciente número de actividades e inversiones de I+D
Aproximadamente 53 medicamentos nuevos se aprobaron en 2020 y 50 en 2021 según los datos proporcionados por el Centro de Evaluación e Investigación de Medicamentos (CDER) de la Administración de Alimentos y Medicamentos (FDA). Entre el total de medicamentos aprobados en todo el mundo en 2020 y 2021, la mayoría de ellos fueron aprobados en los Estados Unidos antes que en cualquier otro país del mundo según la FDA. Además, en cuanto a ensayos clínicos, hasta el año en curso se han registrado 136,276 ensayos clínicos en Estados Unidos, lo que aporta el 31% del total de ensayos clínicos registrados. Se estima que la alta frecuencia de aprobaciones de medicamentos en la región impulsará el crecimiento del mercado en la región durante el período previsto
Además, según los NIH, el presupuesto del presidente incluye 12.100 millones de dólares para el año fiscal 2023 en recursos obligatorios para apoyar la preparación para una pandemia, incluida la investigación y el desarrollo de vacunas, diagnósticos y terapias contra familias virales de alta prioridad, la bioseguridad y la bioprotección, así como para aumentar capacidad de laboratorio e infraestructura de ensayos clínicos en los Estados Unidos. Se espera que este creciente número de ensayos clínicos, el número de aprobaciones de medicamentos y la participación de las principales empresas en mayores gastos en I+D impulsen la demanda de crecimiento del mercado de pruebas analíticas farmacéuticas en la región de América del Norte
Además, las iniciativas estratégicas adoptadas por los actores clave, como lanzamientos de productos, aprobaciones y asociaciones, también están impulsando el crecimiento del segmento. Por ejemplo, en diciembre de 2021, Pace Analytical Services, una división de Pace Science and Technology Company, adquirió Special Pathogens Laboratory para fortalecer sus capacidades en la industria. Se estima que estos acontecimientos impulsarán el crecimiento del mercado en la región