Tendencias del Mercado de Diagnóstico in vitro Industria
Se espera que los reactivos tengan la mayor participación de mercado en el segmento de productos
El segmento de mercado de reactivos incluye componentes, soluciones o preparaciones químicas, biológicas o inmunológicas destinadas por el fabricante a utilizarse durante el proceso de diagnóstico in vitro. Dado el alto costo de muchas plataformas de diagnóstico, es común que los fabricantes arrienden equipos en lugar de vender la tecnología directamente a los usuarios finales. En estos acuerdos, el arrendamiento está vinculado a contratos para comprar reactivos o ensayos asociados para el equipo durante la vida del contrato.
Además, con la creciente carga de enfermedades crónicas en todo el mundo, aumenta la demanda de diagnósticos in vitro, lo que aumenta la demanda de reactivos utilizados en las diversas plataformas de prueba. Según la Décima edición del Atlas de Diabetes de la Federación Internacional de Diabetes de 2021, un total de 537 millones de personas (de 20 a 79 años) en todo el mundo tienen diabetes. En 2030 habrá 643 millones de diabéticos en todo el mundo y en 2045 habrá 783 millones. Se espera que la creciente población afectada por enfermedades crónicas, que requieren pruebas clínicas oportunas para monitorear sus condiciones, impulse el crecimiento del segmento de reactivos durante el período previsto.
Además, se espera que las adquisiciones por parte de actores clave del mercado contribuyan al crecimiento del mercado. Por ejemplo, en marzo de 2022, Medix Biochemica adquirió el 100 % de las acciones de myPOLS Biotec GmbH. Al adquirir myPOLS Biotec, Medix Biochemica amplió su cartera de materias primas para diagnóstico in vitro y aumentó su selección de reactivos para diagnóstico molecular. Esta adquisición aumenta la presencia global de la empresa y proporciona a los clientes capacidades científicas y tecnológicas aún más avanzadas en diagnóstico molecular.
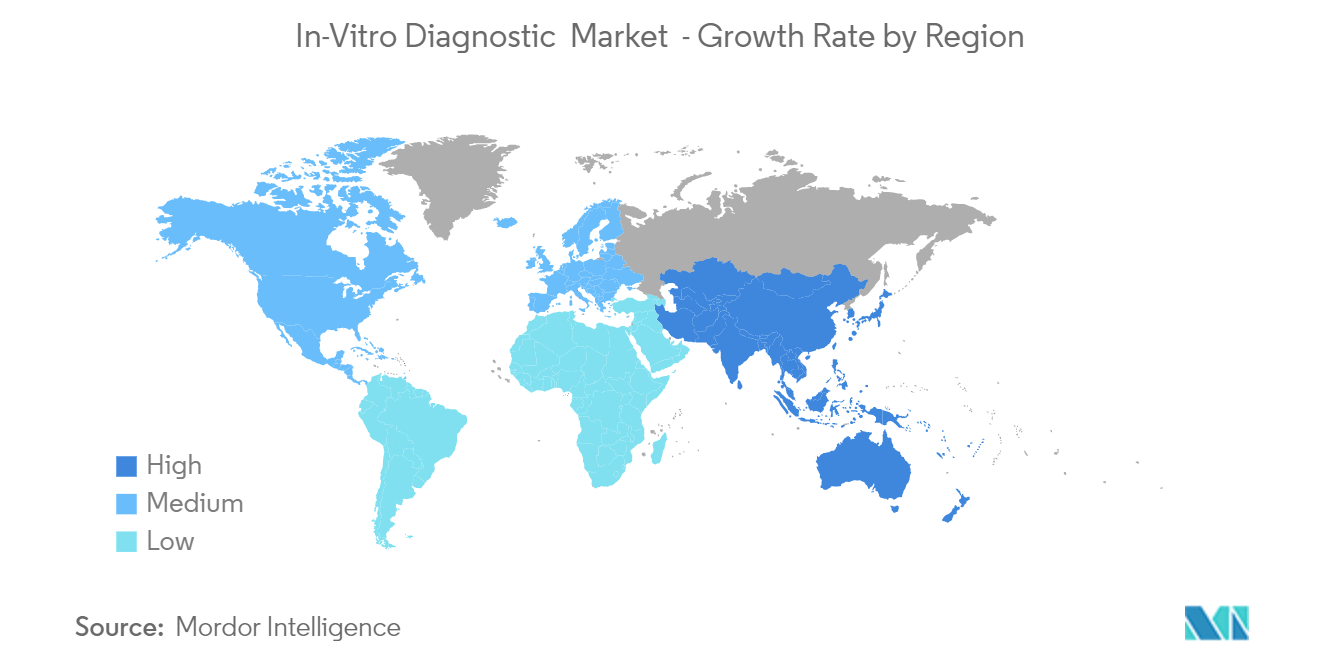
América del Norte domina el mercado y se espera que continúe su dominio durante el período de pronóstico
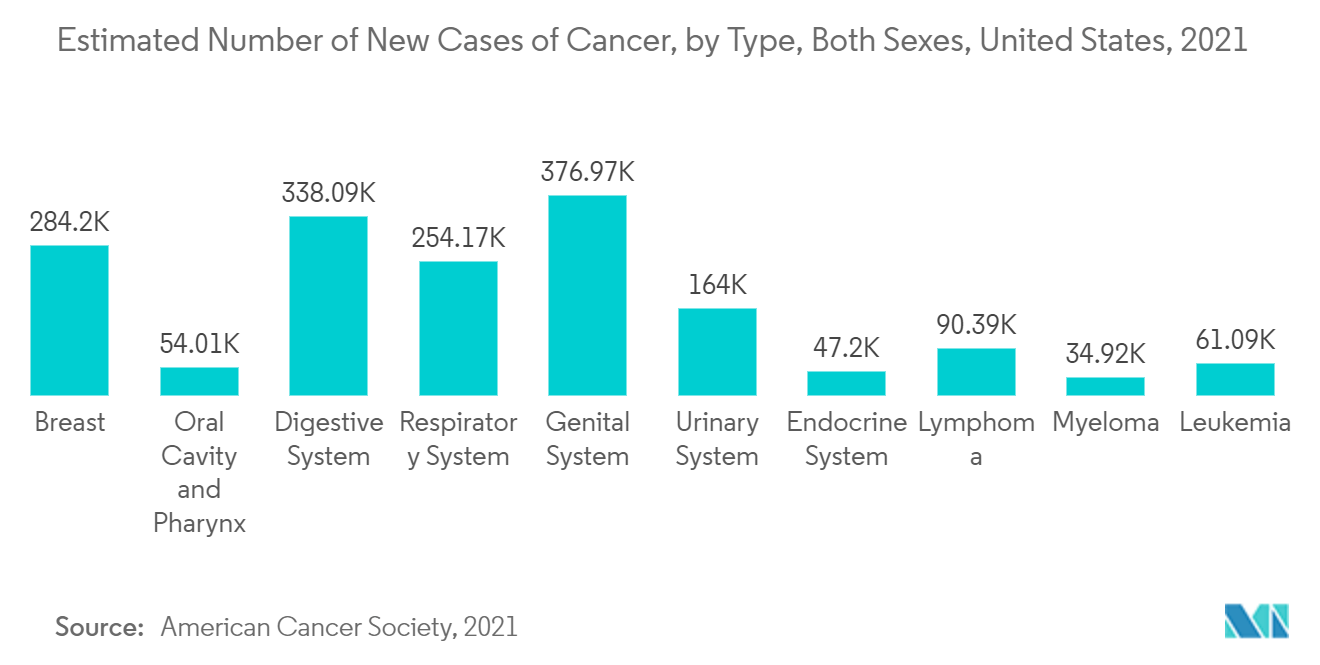
Actualmente, América del Norte tiene un crecimiento significativo en el mercado de IVD y se espera que continúe siendo su fortaleza durante algunos años más. Se espera que esta región aumente su participación de mercado en el futuro, debido a la industria de la salud bien establecida y la creciente prevalencia de enfermedades crónicas. Estados Unidos posee la mayor parte del mercado en la región de América del Norte debido al creciente gasto en atención médica y la rápida adopción de pruebas en el lugar de atención. Según los datos de los Centros para el Control y la Prevención de Enfermedades sobre enfermedades crónicas actualizados en julio de 2022, las enfermedades crónicas son la principal causa de muerte y discapacidad cada año en los Estados Unidos. El creciente número de enfermedades crónicas en el país se suma al crecimiento de los diagnósticos in vitro en el país. Además, según la Sociedad Estadounidense del Cáncer, en enero de 2022, el cáncer sigue siendo la segunda causa de muerte más común en Estados Unidos, después de las enfermedades cardíacas. Se espera que en 2022 se produzcan en Estados Unidos un total de 1,9 millones de nuevos casos de cáncer y 609.360 muertes por cáncer, lo que equivale a unas 1.670 muertes por día. Además, las personas con enfermedades crónicas son los usuarios más frecuentes de los centros de salud en los Estados Unidos. Representan la mayoría de las admisiones hospitalarias y el despacho de recetas y, por lo tanto, impulsan el crecimiento del mercado. La alta carga de enfermedades crónicas y objetivo en la región y la creciente demanda de diagnóstico temprano son los otros factores importantes que están impulsando el crecimiento del mercado estudiado en los Estados Unidos
Además, el creciente número de lanzamientos de productos en la región y la alta concentración de actores clave en América del Norte actúan como factores importantes para impulsar el mercado. Por ejemplo, en mayo de 2020, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) otorgó la Autorización de uso de emergencia (EUA) al kit de prueba de PCR digital en gotas (ddPCR) del SARS-CoV-2 de Bio-Rad Laboratories Inc.. La prueba SARS-CoV-2 Droplet Digital PCR (ddPCR) se ejecuta en los sistemas ddPCR QX200 y QXDx de Bio-Rad