Waise Drogen Marktgröße und -anteil
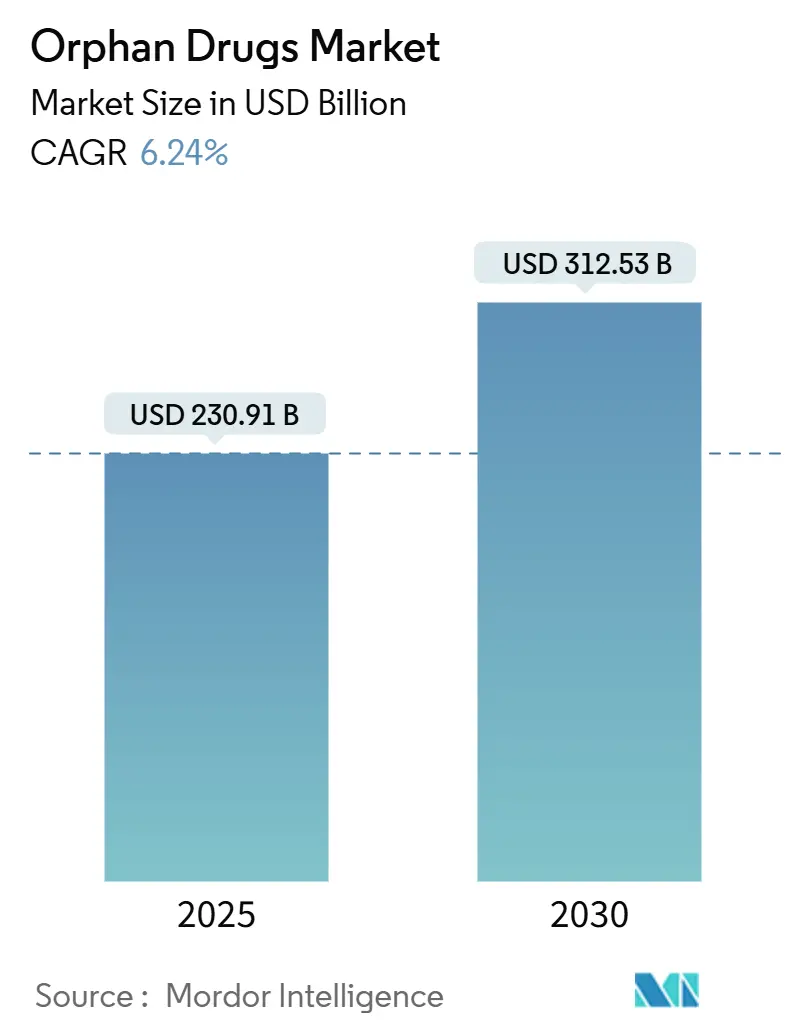
Waise Drogen Marktanalyse von Mordor Intelligenz
Der Waise Drogen Markt betrug USD 230,91 Milliarden im Jahr 2025 und wird voraussichtlich USD 312,53 Milliarden bis 2030 erreichen, mit einem Wachstum von 6,24% CAGR. Das anhaltende Wachstum spiegelt regulatorische Anreize, Gen- und Zelltherapie-Durchbrüche sowie anhaltende unerfüllte Bettürfnisse bei mehr als 7.000 seltenen Krankheiten wider. Die Dominanz von Biologika, insbesondere Gentherapien und monoklonale Antikörper, unterstreicht die Hinwendung zu kurativen einmaligen Behandlungen. Nordamerika führt aufgrund robuster Designationsprogramme und starker Erstattung, während Asien-Pazifik an Dynamik gewinnt, da sich die politischen Rahmenbedingungen erweitern. Die Wettbewerbsdynamik zeigt Große Pharmaunternehmen, die spezialisierte Biotechnologie-Innovatoren akquirieren, um Pipeline-Tiefe zu sichern, und künstliche Intelligenz-gestützte Adaptiv Studien verkürzen Entwicklungszyklen, um erweiterte Exklusivitätszeiträume zu nutzen.
Wichtige Berichts-Erkenntnisse
- Nach Arzneimitteltyp hielten Biologika 65,65% des Waise Drogen Marktanteils im Jahr 2024 und wachsen mit einer CAGR von 8,84% bis 2030.
- Nach Krankheitsbereich führten onkologische Erkrankungen mit 40,53% Umsatzanteil im Jahr 2024, während hämatologische und immunologische Erkrankungen die schnellste CAGR von 10,35% bis 2030 verzeichnen.
- Nach Verabreichungsweg eroberten parenterale Produkte 78,82% Anteil der Waise Drogen Marktgröße im Jahr 2024, jedoch wird für orale Formulierungen eine Expansion mit 11,26% CAGR prognostiziert.
- Nach Vertriebskanal kontrollierten Krankenhausapotheken 68,82% des Umsatzes im Jahr 2024; online-Apotheken repräsentieren das schnellste Wachstum mit 9,26% CAGR.
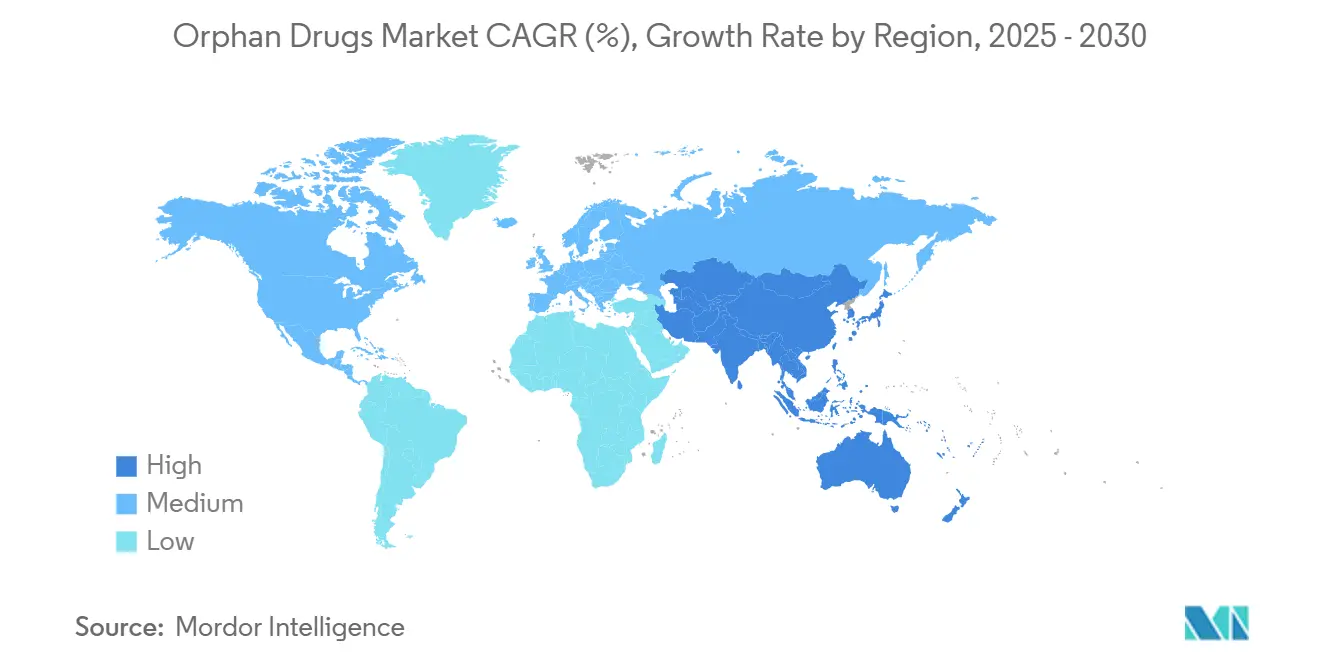
- Nach Geographie behielt Nordamerika 42,82% Anteil des Waise Drogen Marktes im Jahr 2024, während Asien-Pazifik die stärkste CAGR von 11,62% bis 2030 verzeichnen wird.
Globale Waise Drogen Markttrends und Einblicke
Treiber-Auswirkungsanalyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeithorizont |
|---|---|---|---|
| Anstieg von Gen- & Zelltherapie-Plattformen für ultra-seltene Erkrankungen | +2.1% | Nordamerika & EU führend, APAC aufkommend | Mittelfristig (2-4 Jahre) |
| Steigende Prävalenz seltener Krankheiten | +1.8% | Global, höher im alternden Nordamerika & Europa | Langfristig (≥ 4 Jahre) |
| Marktexklusivität für Waise-designierte Arzneimittel | +1.5% | Global, am stärksten In regulierten Märkten | Langfristig (≥ 4 Jahre) |
| Günstige staatliche Anreize & Steuergutschriften | +1.2% | Nordamerika & EU primär, Expansion nach APAC | Mittelfristig (2-4 Jahre) |
| KI-gesteuerte Adaptiv Studien verkürzen Zeitpläne | +0.8% | Global, konzentriert In wichtigen Forschungszentren | Kurzfristig (≤ 2 Jahre) |
| Neupositionierung stillgelegter Phase-II-Assets | +0.6% | Global, getrieben von Pharmaunternehmen | Kurzfristig (≤ 2 Jahre) |
| Quelle: Mordor Intelligence | |||
Anstieg von Gen- & Zelltherapie-Plattformen für Ultra-Seltene Erkrankungen
Gentherapie definiert den Waise Drogen Markt neu, indem sie ursächliche Mutationen anstatt symptomatischer Pfade angreift. Die FDA-Zulassung von KEBILIDI für Aromatische-L-Aminosäure-Decarboxylase-Mangel im November 2024 demonstrierte klinisch bedeutsame motorische Verbesserungen nach einer einzigen Infusion[1]Büro von Die Commissioner, "FDA Approves First Gen Therapie für Behandlung von Aromatic L-Aminosäure Säure Decarboxylase Mangel," fda.gov. Ähnliche Dynamik zeigt sich In Europa, wo LENMELDY 2024 die EMA-Zulassung für metachromatische Leukodystrophie erhielt und beschleunigte Biomarker-gesteuerte Verfahren validierte. Eine Konvergenz von Crisper-Editierung mit Adeno-assoziierten Virus-Lieferung ermöglicht tragfähige Geschäftsmodelle selbst bei globaler Prävalenz unter 1.000 Individuen. Prämie-Preisgestaltung, die USD 2 Millionen pro Kurs überschreiten kann, unterstützt Renditen auf die spezialisierte Infrastruktur, die Hersteller aufbauen müssen. Früheinsteiger mit vertikal integrierten Vektor-Produktionslinien erreichen beeindruckende Eintrittsbarrieren und Preissetzungsmacht.
KI-Gesteuerte Adaptive Studien Verkürzen Entwicklungszeiten
Künstliche-Intelligenz-Plattformen ermöglichen Protokollanpassungen basierend auf Zwischenwirksamkeits- und Sicherheitssignalen, reduzieren Patientenexposition und sparen 18-24 Monate gegenüber festen Designs[2]Aman Mourya, "KI-angetrieben Klinisch Versuche Und regulatory transparency," SpringerLink, springer.com. Der FDA-Workshop zu KI 2024 klärte Dokumentationserwartungen und förderte schnellere, dennoch verantwortliche Wege. Maschine-Lernen-Algorithmen verbessern Patientenstratifizierung, kritisch In Studien, wo Kohorten selten 200 Teilnehmer überschreiten. Sponsoren erreichen dadurch regulatorische Evidenz mit kleineren N-Größen und ermöglichen schnellen Eintritt In den Waise Drogen Markt vor Exklusivitätsabläufen. Große Firmen mit internen Daten-Wissenschaft-Teams dominieren jetzt Adaptiv Studienfähigkeiten und verbreitern die Wettbewerbslücke.
Günstige Staatliche Anreize & Steuergutschriften
Die uns Waise Medikament Tax Credit erstattet 25% der förderfähigen klinischen Kosten, während das FDA-Stipendienprogramm direkt nachweisen-von-Concept-Studien für Krankheiten wie ALS finanziert. Europa gleicht mit 10-jähriger Marktexklusivität und Gebührenerlass aus und hat seit 2000 mehr als 200 Waise-Medikamente zugelassen. Chinas Pflege-Initiative und Indiens nationale Seltene-Krankheiten-Politik erweitern die Anreiz-Reichweite In Asien und reduzieren effektive Projektkosten um bis zu 60% gegenüber traditioneller Entwicklung. Öffentliche Unterstützung unterhält dadurch eine Pipeline, die nun Zustände adressiert, die einst als kommerziell unrentabel galten.
Neupositionierung Stillgelegter Phase-II-Assets für Nischenbereiche
Richtlinien des International selten Krankheiten Forschung Consortium helfen Entwicklern, Verbindungsbibliotheken für neue Seltene-Krankheiten-Matches zu durchsuchen. Empagliflozins Neupositionierung für Lafora-Krankheit exemplifiziert die Strategie, da präklinische Daten neuroprotektive Wirkungen jenseits SGLT2-Hemmung aufdeckten. Bestehende Sicherheitsdossiers verkürzen die Zulassungsuhr um zwei bis drei Jahre, ein Segen für kleinere Biotechs mit knappen Entdeckungsbudgets. Lizenzverträge lassen Originatoren versunkene F&e-Ausgaben retten, während Erwerber schnellen Eintritt In den Waise Drogen Markt mit reduziertem Risiko sichern.
Beschränkungs-Auswirkungsanalyse
| Beschränkung | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeithorizont |
|---|---|---|---|
| Hohe Pro-geduldig-Behandlungskosten | -1.4% | Global, am stärksten In preissensitiven Märkten | Mittelfristig (2-4 Jahre) |
| Zahler-Prüfung bei Indikationserweiterung & real-Welt-Wert | -1.1% | Nordamerika & EU primär | Kurzfristig (≤ 2 Jahre) |
| Begrenzter Patientenpool für Studien & Marketing | -0.9% | Global, akut bei ultra-seltenen Krankheiten | Langfristig (≥ 4 Jahre) |
| Gesetzgebungsvorschläge zur Verkürzung von Exklusivitätsfenstern | -0.8% | USA & EU, potenzieller globaler Spillover | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Hohe Pro-Patient-Behandlungskosten
Die mediane jährliche Therapiekosten überstiegen USD 256.000 In 2024, und einmalige Gentherapien überschreiten häufig USD 2 Millionen. Zahler reagieren mit Vorautorisierung und ergebnisbasierten Verträgen, besonders wenn Behandlungen später In breitere Populationen expandieren. Europäische HTA-Gremien fordern zunehmend Post-Launch-Evidenz dauerhaften Nutzens und drängen Sponsoren dazu, langfristige Register zu finanzieren, die materielle Kosten hinzufügen. Preisstrategie bleibt daher ein delikates Gleichgewicht zwischen Rückgewinnung von Innovationsinvestitionen und Aufrechterhaltung der Erstattungsviabilität.
Zahler-Prüfung bei "Indikationserweiterung"
Der Inflation Reduktion Act erlaubt Preisneuverhandlung, sobald ein Medikament Nicht-Waise-Indikationen sichert, entmutigt Expansion und schärft Fokus auf Wertdemonstration. Ergebnisbasierte Vereinbarungen In Europa spiegeln diese Haltung wider und knüpfen Erstattung an real-Welt-Wirksamkeit. Pharmaunternehmen müssen nun Gesundheitsökonomie-Studien früh In der Entwicklung budgetieren, um Zugang zu bewahren, und einige Pipelines werden von inkrementellen Indikationen weg umpriorisiert, um Margenerosion zu vermeiden.
Segment-Analyse
Nach Arzneimitteltyp: Biologika Führen Innovationswelle
Biologika machten 65,65% des Umsatzes In 2024 aus und werden kleine Moleküle mit einer CAGR von 8,84% bis 2030 überholen. Fünfundzwanzig Prozent der FDA-Zulassungen 2024 waren monoklonale Antikörper oder Gentherapien, was anhaltende Präferenz für Modalitätsplattformen signalisiert, die Präzisionsinterventionen ermöglichen. Die Waise Drogen Marktgröße für Biologika wird voraussichtlich USD 205 Milliarden bis 2030 erreichen, getragen von einmaligen kurativen Therapien, die Prämie-Preise verlangen. Nicht-Biologika behalten noch Anteile In Stoffwechselstörungen über neupositionierte kleine Moleküle, doch die Wettbewerbsdifferenzierung verengt sich, da genetische Medikamente zugrunde liegende enzymatische Defizite effektiver adressieren. Hersteller, die virale Vektor-Anlagen skalieren, gewinnen Kostenhebel, während kleine-Molekül-Produzenten auf Formulierungsinnovation und Lebenszyklus-Management angewiesen sind, um relevant zu bleiben.
Zweiter Absatz: Gentherapie-Exemplare umfassen LYFGENIA für Sichelzellkrankheit und KEBILIDI für aromatische L-AAD-Mangel, beide demonstrieren transformativen klinischen Nutzen mit einmaligen Verabreichungen. Herstellungskomplexität erhöht Eintrittsbarrieren; folglich sind CDMO-Partnerschaften und interne Vektorkapazität zu Akquisitionsauslösern geworden. Regulierungsbehörden verlangen robuste Potenz-Tests und langfristige Nachverfolgung, was Unternehmen dazu veranlasst, multidisziplinäre Überwachungsprogramme zu etablieren. Geistige-Eigentum-Strategien fokussieren auf breite Plattform-Patente um Kapsid-Maschinenbau und Promotor-Optimierung und konsolidieren dadurch Wettbewerbsgräben innerhalb des Waise Drogen Marktes.
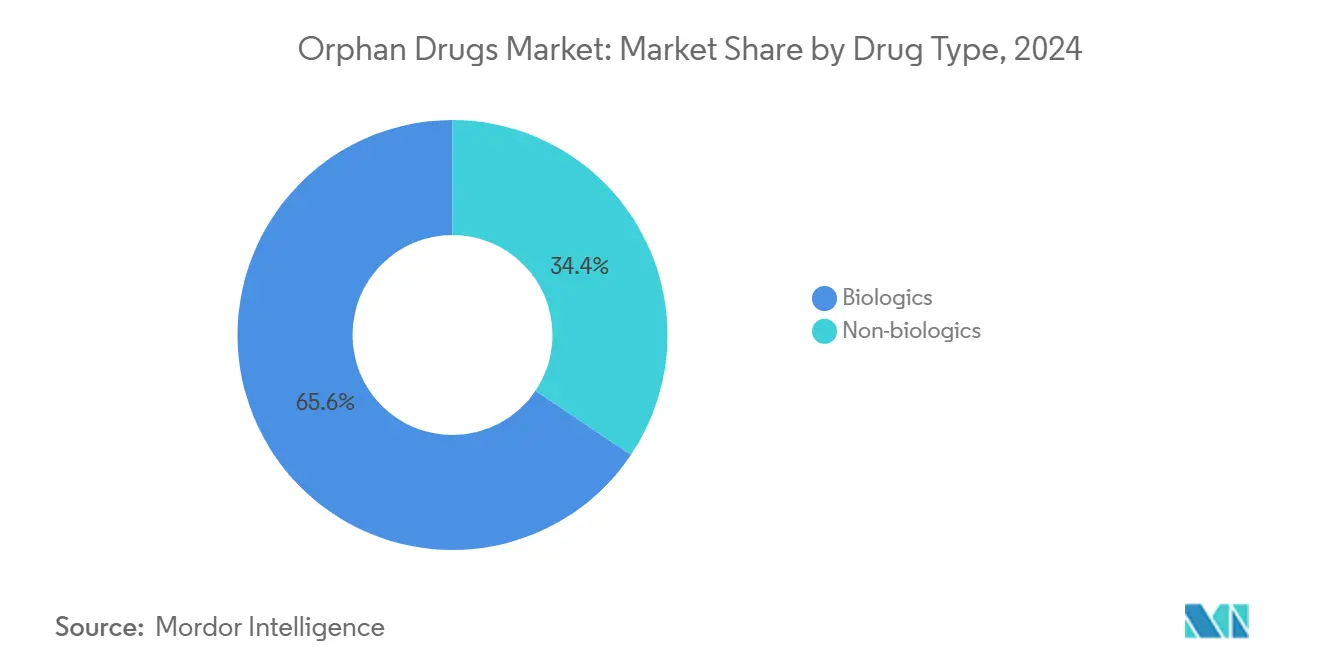
Notiz: Segmentanteile aller Einzelsegmente bei Berichtskauf verfügbar
Nach Krankheitsbereich: Onkologische Dominanz Steht Hämatologischer Herausforderung Gegenüber
Onkologische Erkrankungen behielten 40,53% Anteil In 2024, zeigen aber langsameres Wachstumstempo, da Sättigung In hämatologischen Malignomen auftritt. Der Waise Drogen Marktanteil für Onkologie betrug 41% In 2024 und wird voraussichtlich marginal sinken, während neuere Kategorien beschleunigen. EMA-Zulassung von Ordspono für rezidivierendes follikuläres Lymphom unterstreicht anhaltende Innovation In T-Zell-umleitenden Antikörpern. Jedoch schreiten hämatologische und immunologische Erkrankungen mit einer CAGR von 10,35% voran, angetrieben von Faktor-Ersatz-Alternativen wie Concizumab und Fitusiran.
Zweiter Absatz: Neurologische Gentherapien, einschließlich Tofersen für SOD1-ALS, erweitern die Pipeline und heben Biomarker-gesteuerte Zulassungen hervor. Stoffwechselkrankheiten-Programme nutzen nächste Generation Enzym-Ersatz und mRNA-Therapie, während Infektionskrankheiten-Seltenheiten wie virale hämorrhagische Fieber Nischen-Finanzierung anziehen. Investoren verfolgen therapeutische Neuheit und regulatorische Dynamik bei der Bewertung von Portfolio-Gewichtungen über diese Segmente.
Nach Verabreichungsweg: Orale Innovation Fordert Parenterale Dominanz Heraus
Parenterale Modalitäten hielten 78,82% Umsatzanteil In 2024 aufgrund der Stabilitätsbedürfnisse von Biologika. Dennoch werden orale Formate für eine CAGR von 11,26% prognostiziert, da Nano-Träger und Permeabilitätsverstärker-Technologien voranschreiten. Die Waise Drogen Marktgröße für orale Formulierungen wird voraussichtlich USD 35 Milliarden bis 2030 überschreiten. Klinische Erfolge In Peptid-Absorption mit pH-responsiven Beschichtungen validieren frühere präklinische Befunde. Patientenpräferenz-Umfragen zeigen, dass 72% der primären Hyperoxalurie-Patienten selbst-verabreichte Optionen bevorzugen, was Sponsoren incentiviert, bestehende Injektionen zu oralen Alternativen zu re-engineeren.
Zweiter Absatz: Gerät-assistierte subkutane Infusoren und Implantate diversifizieren die Lieferung weiter und unterstützen chronische Regime In immunologischen Zuständen. Inhalierte Biologika adressieren pulmonale seltene Krankheiten, obwohl Kühlketten-Anforderungen herausfordernd bleiben. liefern-Kette-Digitalisierung und häusliche Pflegemodelle reduzieren Krankenhausressourcen-Belastungen und stimmen mit Gesundheitssystem-Imperativen für Kosteneindämmung überein.
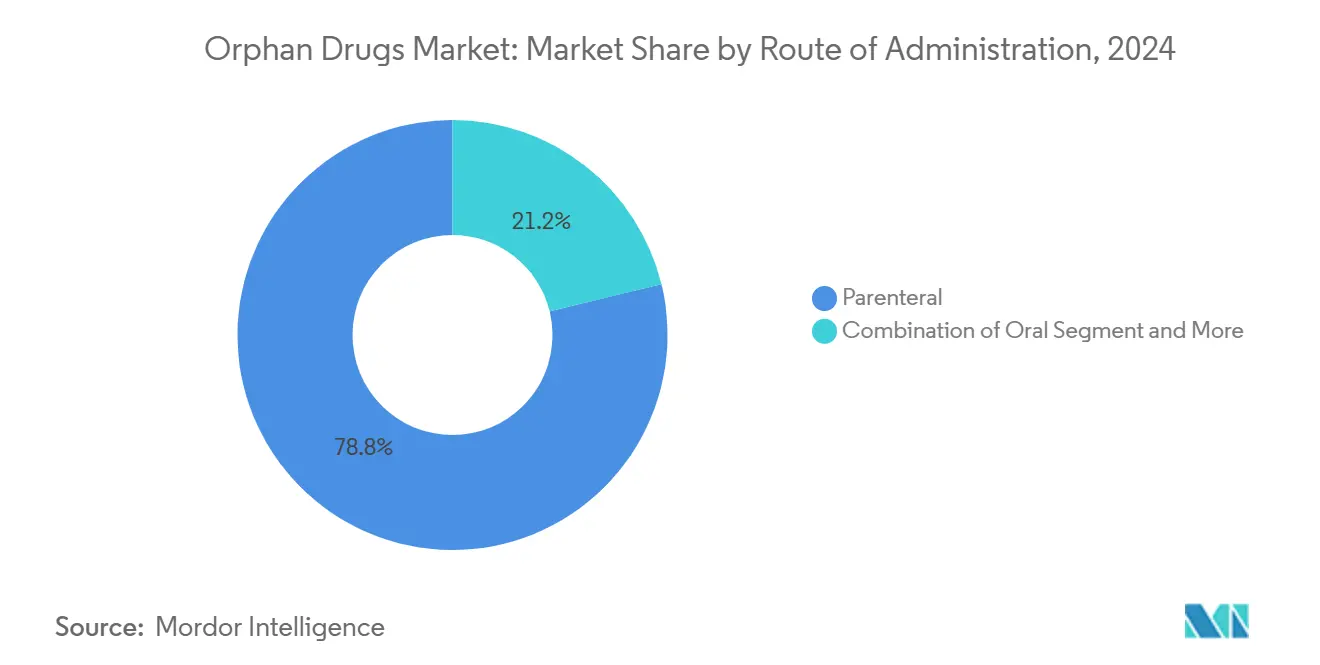
Notiz: Segmentanteile aller Einzelsegmente bei Berichtskauf verfügbar
Nach Vertriebskanal: Spezialnetzwerke Treiben Online-Wachstum
Krankenhausapotheken beherrschten 68,82% der Verkäufe In 2024, da komplexe Handhabungsprotokolle zentrumsbasierte Dispensierung begünstigen. Dennoch wachsen online-Spezial-Hubs jährlich um 9,26% und nutzen Telehealth und direkte Patientenlogistik. Integrierte Modelle, wie Lurie Childrens geplante pädiatrische Spezialapotheke, illustrieren Konvergenz klinischer Expertise mit Last-Mile-Lieferung.
Zweiter Absatz: Einzelhandelskanäle bleiben auf orale Therapien und unterstützende Medikamente beschränkt, dennoch ermöglichen Partnerschaften mit Spezialapotheken erweiterte therapeutische Angebote ohne bedeutende Infrastruktur-Upgrades. Blockchain-basierte Schiene-Und-verfolgen-Systeme verbessern Temperaturmonitoring und Fälschungsminderung. Da Zahlerverträge zunehmend Arzneimittel- und Dienstleistung-Erstattung bündeln, gewinnen Spezialnetzwerke, die Adhärenz-Programme bereitstellen, Verhandlungshebelwirkung über den Waise Drogen Markt.
Geographie-Analyse
Nordamerika eroberte 42,82% des globalen Umsatzes In 2024 und profitiert weiterhin von 7-jähriger Exklusivität unter dem Waise Medikament Act plus der 25% Klinische-Studien-Steuergutschrift[3]Jonathan Cardella, "Waise Drogen & Die R&D Tax Credit," StrikeTax.com, striketax.com. Kürzliche FDA-Zulassungen von XOLREMDI für WHIM-Syndrom und RYT-ELO für Hochrisiko-myelodysplastische Syndrom illustrieren Regulatoren-Responsivität. Dennoch führt der Inflation Reduktion Act Preisneuverhandlungsrisiko ein, wenn Produkte über einzelne Waise-Indikationen hinaus expandieren, was strategische Vorsicht bei Etikett-Erweiterungen veranlasst.
Europa hält einen bedeutenden Anteil des Waise Drogen Marktes aufgrund zentralisierter EMA-Verfahren, die 10-jährige Exklusivität und Gebührenerleichterung bieten. Das Kritisch Medikamente Act sucht regionale Herstellungsresilienz aufzubauen und Engpässe zu straffen, aber Entwurfsreformen schlagen vor, regulatorischen Datenschutz auf neun Jahre zu reduzieren, was potentiell Investitionsenthusiasmus Dämpft. Gemanagt-Eintrag-Vereinbarungen und ergebnisbasierte Verträge dominieren Zahlerverhandlungen und sichern Zugang bei kontrollierter Ausgabe.
Asien-Pazifik ist die am schnellsten wachsende Region mit 11,62% CAGR bis 2030, unterstützt durch das Pflege-Programm In China und Indiens Seltene-Krankheiten-Politik-Zuschüsse. Die Großen Populationen der Region erleichtern Studienrekrutierung, und steigende verfügbare Einkommen unterstützen Prämie-Therapien. Dennoch begrenzen fragmentierte Erstattung und Variabel epidemiologische Daten sofortige Aufnahme und erfordern von Sponsoren die Entwicklung lokalisierter Engagement-Strategien.
Wettbewerbslandschaft
Der Waise Drogen Markt zeigt moderate Fragmentierung, da Große Pharmaunternehmen Nischen-Innovatoren für differenzierte Assets akquirieren. Johnson & Johnson, Novartis und Roche halten gemeinsam bedeutenden Umsatzanteil, während Dutzende kleinerer Biotechs Pipeline-Neuheit liefern. Sanofis geplante USD 300 Millionen Partnerschaft mit Orano Med zielt auf Radioligand-Therapien für seltene Krebsarten und spiegelt einen Trend zur Modalitätsdiversifikation wider.
M&eine-Volumina blieben durch Anfang 2025 erhöht, mit der Mallinckrodt-Endo-Fusion, die auf operative Skalierung und komplementäre Marken wie XIAFLEX und Acthar Gel abzielt. Strategische Kooperationen helfen Herstellungsrisiko In Gentherapie zu mindern; Novartis' Investment In virale Vektor-CDMOs exemplifiziert vertikal-integrative Ambitionen. KI-Kompetenz ist als strategischer Differenziator aufgetaucht und veranlasst Talentakquisition und akademische Partnerschaften zur Verbesserung datengetriebener Studiendesigns.
Geistige-Eigentum-Strategien betonen breite Plattform-Patente um Vektor-Maschinenbau und Promotor-Sequenzen und erweitern dadurch Schutzgräben über einzelne Assets hinaus. Markteintretende stehen vor hoher Kapitalintensität für GMP-Vektor-Anlagen und langfristigen Sicherheitsüberwachungsverpflichtungen, was Incumbents' Vorteil verstärkt. Da Regulatoren Post-Markt-Evidenz fordern, genießen Firmen mit real-Welt-Daten-Infrastruktur glattere Erneuerungen und Etikett-Expansionen.
Waise Drogen Branchenführer
-
Takeda Pharmazeutisch Company Limited
-
Novartis AG
-
Johnson & Johnson
-
F. Hoffmann-La Roche Ltd
-
Bristol-Myers Squibb Co.
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Aktuelle Branchenentwicklungen
- März 2025: Mallinckrodt und Endo kündigten Fusion an, um einen diversifizierten Pharmaführer mit Fokus auf seltene Krankheiten zu schaffen.
- Dezember 2024: FDA genehmigte Alhemo (Concizumab-mtci) für Prophylaxe bei Hämophilie eine oder B Patienten mit Inhibitoren.
- November 2024: FDA genehmigte KEBILIDI, die erste Gentherapie für aromatischen L-AAD-Mangel.
Globaler Waise Drogen Marktbericht-Umfang
Entsprechend dem Berichtsumfang können Waise Drogen als Moleküle definiert werden, die zur Behandlung einer seltenen Krankheit bestimmt sind. Die seltene Krankheit hat, wie der Name schon sagt, eine niedrige Prävalenzrate und wurde In verschiedenen geografischen Regionen unterschiedlich definiert. Der Waise Drogen Markt ist segmentiert nach Arzneimitteltyp (Biologisch, Nicht-biologisch), Meistverkaufte Medikamente (Revlimid, Darzalex, Rituxan, Tafinlar, Ninlaro, Imbruvica, Myozyme, Soliris, Jakafi, Kyprolis, Andere Meistverkaufte Medikamente), Krankheitstyp (Onkologie, Hämatologie, Neurologie, Kardiovaskulär, Andere Krankheitstypen) und Geographie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika, und Südamerika). Der Marktbericht deckt auch die geschätzten Marktgrößen und Trends für 17 verschiedene Länder In wichtigen Regionen weltweit ab. Der Bericht bietet den Wert (In USD Millionen) für die oben genannten Segmente.
| Biologika |
| Nicht-Biologika |
| Onkologische Erkrankungen |
| Hämatologische & Immunologische Erkrankungen |
| Neurologische Erkrankungen |
| Stoffwechselerkrankungen |
| Infektionskrankheiten |
| Andere Seltene Krankheiten |
| Parenteral |
| Oral |
| Andere (Inhalation, Topisch, Implantierbar) |
| Krankenhausapotheken |
| Einzelhandelsapotheken |
| Online-Apotheken |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Übriges Europa | |
| Asien-Pazifik | China |
| Japan | |
| Indien | |
| Südkorea | |
| Australien | |
| Übriger Asien-Pazifik-Raum | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Übriger Naher Osten und Afrika | |
| Südamerika | Brasilien |
| Argentinien | |
| Übriges Südamerika |
| Nach Arzneimitteltyp | Biologika | |
| Nicht-Biologika | ||
| Nach Krankheitsbereich | Onkologische Erkrankungen | |
| Hämatologische & Immunologische Erkrankungen | ||
| Neurologische Erkrankungen | ||
| Stoffwechselerkrankungen | ||
| Infektionskrankheiten | ||
| Andere Seltene Krankheiten | ||
| Nach Verabreichungsweg | Parenteral | |
| Oral | ||
| Andere (Inhalation, Topisch, Implantierbar) | ||
| Nach Vertriebskanal | Krankenhausapotheken | |
| Einzelhandelsapotheken | ||
| Online-Apotheken | ||
| Geographie | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Übriges Europa | ||
| Asien-Pazifik | China | |
| Japan | ||
| Indien | ||
| Südkorea | ||
| Australien | ||
| Übriger Asien-Pazifik-Raum | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Übriger Naher Osten und Afrika | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Übriges Südamerika | ||
Schlüsselfragen Beantwortet im Bericht
Wie Groß ist der aktuelle globale Waise Drogen Markt und wie schnell wächst er?
Der Markt ist mit USD 230,91 Milliarden In 2025 bewertet und wird voraussichtlich USD 312,53 Milliarden bis 2030 erreichen, was eine CAGR von 6,24% widerspiegelt.
Welcher Arzneimitteltyp hält den größten Anteil des Waise Drogen Marktes?
Biologika führen mit 65,65% Marktanteil In 2024 und expandieren mit einer CAGR von 8,84% bis 2030.
Welche Region wird voraussichtlich am schnellsten im Waise Drogen Markt wachsen?
Asien-Pazifik wird voraussichtlich die stärkste CAGR von 11,62% zwischen 2025 und 2030 verzeichnen.
Was ist der primäre Wachstumstreiber für den Waise Drogen Markt?
Durchbruch-Gen- und Zelltherapie-Plattformen, die ultra-seltene Erkrankungen angreifen, fügen etwa 2,1 Prozentpunkte zur Markt-CAGR hinzu.
Was ist die bedeutendste Beschränkung, die die Marktexpansion beeinflusst?
Hohe Pro-geduldig-Behandlungskosten-oft über USD 300.000 pro Jahr oder USD 2 Millionen für einmalige Gentherapien-üben Abwärtsdruck auf die Adoption aus.
Wie beeinflusst künstliche Intelligenz die Waise Medikament-Entwicklung?
KI-gestützte Adaptiv klinische Studien verkürzen Entwicklungszeiten um 18-24 Monate und helfen Sponsoren, den Markt früher zu erreichen, während sie robuste Evidenzstandards aufrechterhalten.
Seite zuletzt aktualisiert am: