Markt-Trends von Nordamerika Diagnose und Behandlung von Gebärmutterkrebs Industrie
Das Segment Immuntherapie wird im Prognosezeitraum voraussichtlich ein beträchtliches Wachstum verzeichnen
Bei der Immuntherapie handelt es sich um eine Behandlung, bei der Medikamente dem Immunsystem einer Person helfen, Krebszellen zu erkennen und abzutöten. Eine Immuntherapie wird zur Behandlung bestimmter Formen von Gebärmutterschleimhautkrebs durchgeführt, die sich ausgebreitet haben oder erneut aufgetreten sind. Bei der Immuntherapie handelt es sich um eine Behandlung, die das Immunsystem einer Person zur Krebsbekämpfung nutzt. Eine Immuntherapie kann die Funktionsweise des Immunsystems bei der Suche und Bekämpfung von Krebszellen stärken oder verändern. Die Immuntherapie stimuliert die endogene Immunantwort, insbesondere gegen Tumorzellen, und ist die neue Grenze der Krebsbehandlung. Es stehen mehrere Verbindungen zur Verfügung, die auf unterschiedliche biologische Wege abzielen. Einige dieser Wirkstoffe sind bereits für die Behandlung nicht-gynäkologischer bösartiger Erkrankungen wie Lungenkrebs und Melanom zugelassen. Auch bei der Behandlung von Gebärmutterkrebs könnten sie eine wichtige Rolle spielen
Zunehmende Produktzulassungen und zunehmende Produkteinführungen sind die Haupttreiber für das Segmentwachstum. Beispielsweise hat Karyopharm Therapeutics Inc., ein kommerzielles Pharmaunternehmen, das Pionierarbeit bei neuartigen Krebstherapien leistet, im März 2022 ein Update zu seinen Gesprächen mit der US-amerikanischen Food and Drug Administration (FDA) über seinen zuvor geplanten ergänzenden New Drug Application (sNDA) bereitgestellt. Der Antrag basiert auf den Daten der Phase-3-SIENDO-Studie, in der Selinexor als Erstlinien-Erhaltungstherapie nach einer Chemotherapie bei Patienten mit fortgeschrittenem oder rezidivierendem Endometriumkarzinom untersucht wird. In ähnlicher Weise genehmigte die Food and Drug Administration im März 2022 Pembrolizumab (Keytruda, Merck) als Einzelwirkstoff für Patienten mit fortgeschrittenem Endometriumkarzinom, das eine hohe Mikrosatelliteninstabilität (MSI-H) oder einen Mismatch-Reparatur-Defekt (dMMR) aufweist, wie von festgestellt einem von der FDA zugelassenen Test, bei denen es nach vorheriger systemischer Therapie in irgendeinem Umfeld zu einem Fortschreiten der Erkrankung kommt und die nicht für eine kurative Operation oder Bestrahlung in Frage kommen. Daher wird erwartet, dass das Segment aufgrund solcher Fälle im Prognosezeitraum ein beträchtliches Segmentwachstum verzeichnen wird
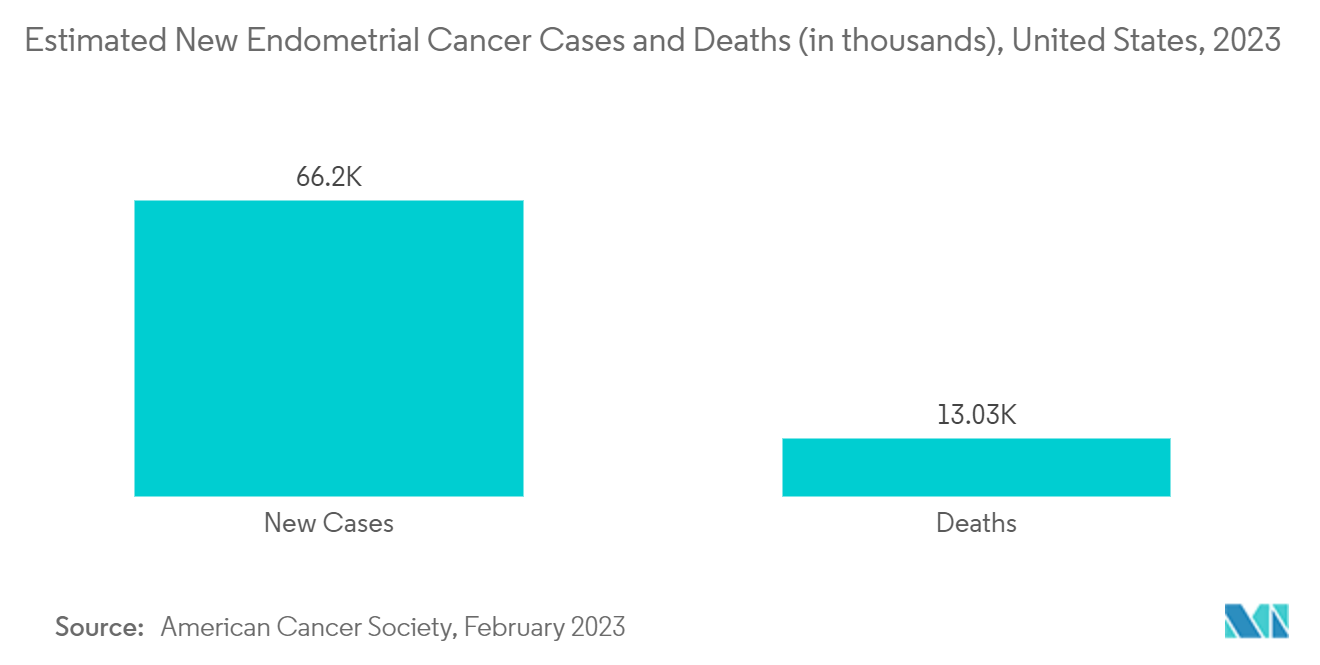
Für die Vereinigten Staaten wird im Prognosezeitraum ein beträchtliches Wachstum erwartet
Wichtige Produkteinführungen, eine hohe Konzentration von Marktteilnehmern oder Herstellerpräsenz, Akquisitionen und Partnerschaften zwischen wichtigen Akteuren sowie steigende Gesundheitsausgaben in den Vereinigten Staaten sind einige Faktoren, die das Wachstum des US-amerikanischen Marktes für die Diagnostik und Behandlung von Gebärmutterkrebs vorantreiben. Beispielsweise wurden laut United States Research and Development Funding and Performance Fact Sheet, 2022, die FE-Ausgaben in den Vereinigten Staaten im Jahr 2021 auf 580 Milliarden US-Dollar geschätzt, wovon 96,5 Milliarden US-Dollar in die Grundlagenforschung investiert wurden, also 115,0 Milliarden US-Dollar auf angewandte Forschung und 368,5 Milliarden US-Dollar wurden im Entwicklungssektor eingesetzt. Es wird erwartet, dass solch hohe Investitionen die Forschung, Entwicklung und Zulassung von Medikamenten gegen Gebärmutterkrebs im Land beschleunigen und das Marktwachstum ankurbeln
Es wird erwartet, dass auch die zunehmenden Produktzulassungen und -einführungen im Land das Marktwachstum steigern werden. Beispielsweise erhielten Myovant Sciences und Pfizer im August 2022 in den USA die FDA-Zulassung für MYFEMBREE, eine einmal täglich einzunehmende Behandlung zur Behandlung mittelschwerer bis starker Schmerzen im Zusammenhang mit Endometriose. MYFEMBREE ist auch für die Behandlung starker Menstruationsblutungen im Zusammenhang mit Uterusmyomen bei Frauen vor der Menopause zugelassen. Myovant und Pfizer werden die gemeinsame Vermarktung von MYFEMBREE in den Vereinigten Staaten fortsetzen und das Produkt wird ab sofort verfügbar sein. Aufgrund dieser Faktoren wird erwartet, dass der Markt des Landes erheblich wachsen wird