Markt-Trends von Behandlung des Myelodysplastischen Syndroms (MDS). Industrie
Es wird erwartet, dass das Stammzelltransplantationssegment einen großen Marktanteil auf dem Markt für die Behandlung des Myelodysplastischen Syndroms (MDS) halten wird
Für Patienten mit myelodysplastischen Syndromen bietet die Stammzelltransplantation (SZT) eine potenziell vorteilhafte Therapie. Es gibt zwei Haupttypen der SCT eine ist eine allogene Stammzelltransplantation und die andere ist eine autologe Stammzelltransplantation. Bei einer allogenen Stammzelltransplantation erhält der Patient nach der Zerstörung des Knochenmarks blutbildende Stammzellen von einer anderen Person, dem Spender. Dies ist die häufigste Transplantationsart bei MDS. Beispielsweise kam die im August 2021 auf PubMed.gov veröffentlichte Studie mit dem Titel Allogene Stammzelltransplantation kann die nachteiligen Auswirkungen von Myelofibrose auf die Prognose des myelodysplastischen Syndroms überwinden zu dem Schluss, dass Patienten mit Myelofibrose (MF)-2/3 eine schlechtere Prognose hatten als diejenigen mit Myelofibrose (MF)-0/1 bei Patienten ohne allogene hämatopoetische Stammzelltransplantation (allo-HSCT)
Allogene SCTs können jedoch schwerwiegende, sogar lebensbedrohliche Nebenwirkungen haben; Daher werden sie normalerweise bei jüngeren, gesünderen Patienten durchgeführt. Patienten in ihren 60ern und sogar 70ern hatten erfolgreiche Transplantationen, bei älteren Patienten wird die SCT jedoch normalerweise mit einer weniger intensiven (reduzierter Intensität) Chemotherapie und/oder Bestrahlung durchgeführt. Niedrigere Dosen töten möglicherweise nicht alle Knochenmarkszellen ab, reichen aber gerade aus, damit Spenderzellen Wurzeln schlagen und im Knochenmark wachsen können. Durch die niedrigeren Dosen treten auch weniger Nebenwirkungen auf, wodurch diese Art der Transplantation für ältere Patienten verträglicher ist. Dennoch bleiben einige schwerwiegende Nebenwirkungen möglich
Zusätzlich erhalten Patienten nach einer autologen Stammzelltransplantation eigene Stammzellen (die vor der Behandlung entnommen wurden). Da das Knochenmark des Patienten abnormale Stammzellen enthält, wird diese Art der Transplantation bei MDS-Patienten selten eingesetzt
Daher wird erwartet, dass die oben genannten Faktoren das Wachstum des Segments im Analysezeitraum beeinflussen werden
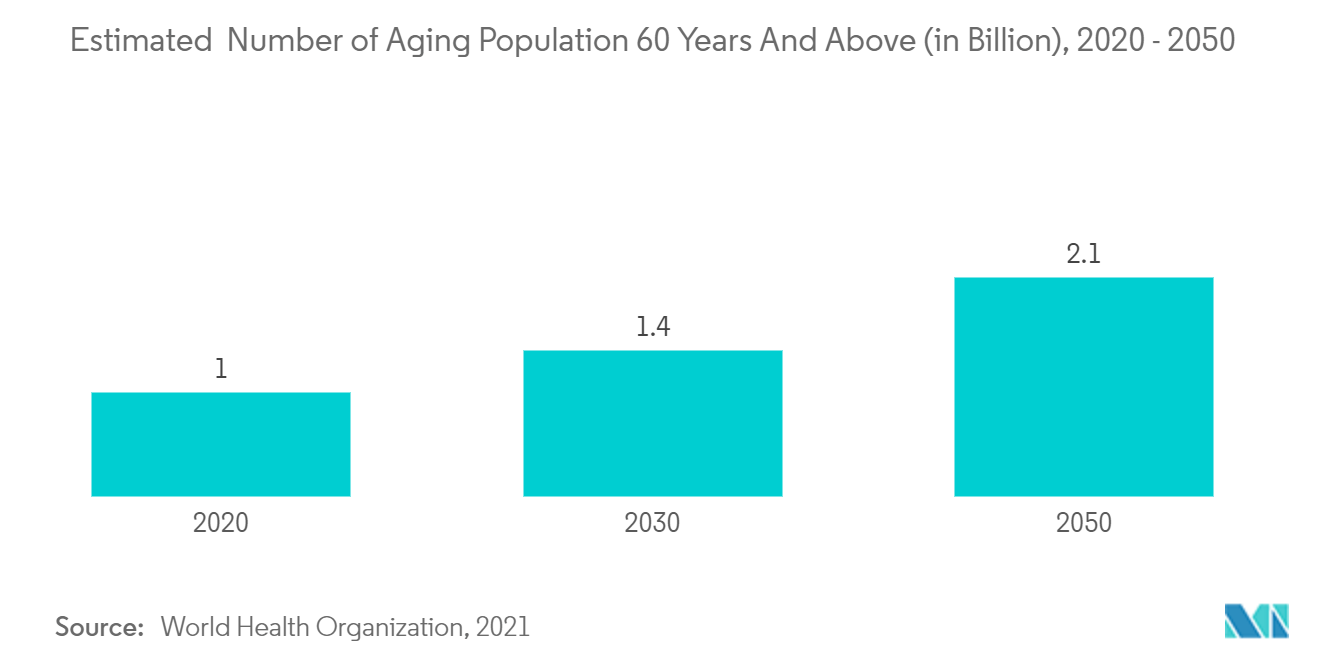
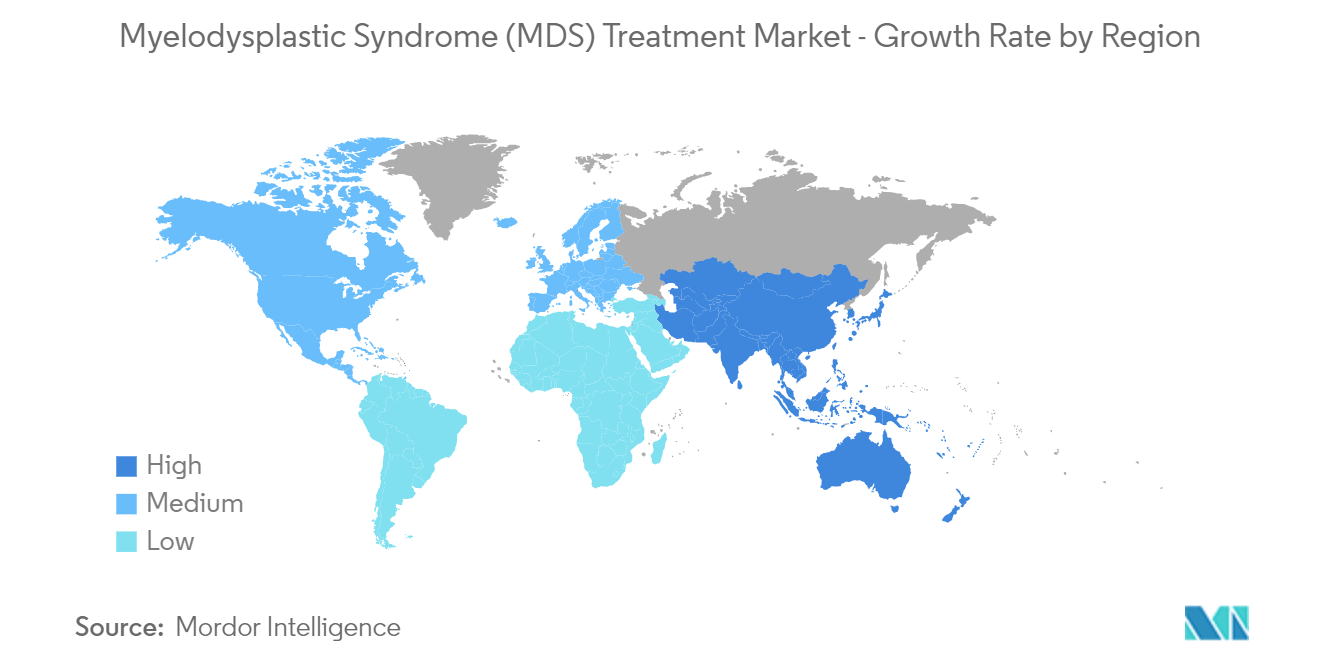
Es wird erwartet, dass Nordamerika einen erheblichen Marktanteil hält und dies auch im Prognosezeitraum tun wird.
Nordamerika dominiert den globalen Markt für die Behandlung des myelodysplastischen Syndroms (MDS), da die Prävalenz des myelodysplastischen Syndroms zunimmt, neuartige Behandlungen frühzeitig eingeführt werden, hohe FE-Investitionen in die Entwicklung neuartiger Medikamente getätigt werden und eine hochentwickelte Gesundheitsinfrastruktur vorhanden ist. Nach Angaben der American Society of Clinical Oncology (ASCO) 2022 sind in den Vereinigten Staaten jedes Jahr etwa 10.000 Menschen von MDS betroffen. MDS ist bei Menschen unter 50 Jahren selten. Menschen in den 70ern erkranken jedoch am häufigsten daran. Es wird erwartet, dass die Zahl der Menschen, bei denen jedes Jahr MDS diagnostiziert wird, mit zunehmendem Alter der US-Bevölkerung steigt
Darüber hinaus nehmen die Produktzulassungen rasant zu, was das Marktwachstum vorantreibt. Takeda Pharmaceutical Company Limited gab beispielsweise im Juli 2020 bekannt, dass die FDA ihrem Prüfpräparat Pevonedistat den Status Breakthrough Therapy für die Behandlung von Patienten mit myelodysplastischen Syndromen mit höherem Risiko (HR-MDS) verliehen hat. Pevonedistat, ein erstklassiger Inhibitor des NEDD8-aktivierenden Enzyms (NAE), könnte die erste neue Behandlung für HR-MDS-Patienten seit über einem Jahrzehnt sein und die Behandlungsmöglichkeiten erweitern, die bisher auf die HMA-Monotherapie beschränkt waren. Selbst mit den aktuellen Behandlungsmöglichkeiten haben Menschen mit HR-MDS weiterhin schlechte Ergebnisse. Ebenso gab Novartis im November 2021 bekannt, dass die US-amerikanische Food and Drug Administration (FDA) Sabatolimab (MBG453) zur Behandlung erwachsener Patienten mit myelodysplastischen Syndromen (MDS), definiert durch eine IPSS-R-Risikokategorie, eine beschleunigte Zulassung erteilt hat mit hohem oder sehr hohem Risiko in Kombination mit hypomethylierenden Arzneimitteln. In ähnlicher Weise gab Gilead Sciences, Inc. im September 2020 bekannt, dass die US-amerikanische Food and Drug Administration (FDA) Magrolimab, einen erstklassigen monoklonalen Anti-CD47-Antikörper seiner Klasse, zur Behandlung des neu diagnostizierten myelodysplastischen Syndroms zugelassen hat Bezeichnung Durchbruchstherapie
Darüber hinaus wird erwartet, dass das steigende Patientenbewusstsein in den Vereinigten Staaten das Marktwachstum im Prognosezeitraum vorantreiben wird. Beispielsweise kündigte Jazz Pharmaceuticals plc im September 2020 den Start von Find the Right Fit an, einem Patientenaufklärungsprogramm in den Vereinigten Staaten, das in Zusammenarbeit mit der Myelodysplastic Syndromes (MDS) Foundation, Inc. und der Cancer Support Community entwickelt wurde, um Menschen dabei zu unterstützen sekundäre akute myeloische Leukämie (sAML) und MDS
Diese Faktoren zusammen dürften das Wachstum des Marktes für die Behandlung des myelodysplastischen Syndroms (MDS) in der nordamerikanischen Region fördern