Größe und Anteil des globalen Marktes für Medizinprodukte-Prüfung und -Zertifizierung
Analyse des globalen Marktes für Medizinprodukte-Prüfung und -Zertifizierung von Mordor Intelligence
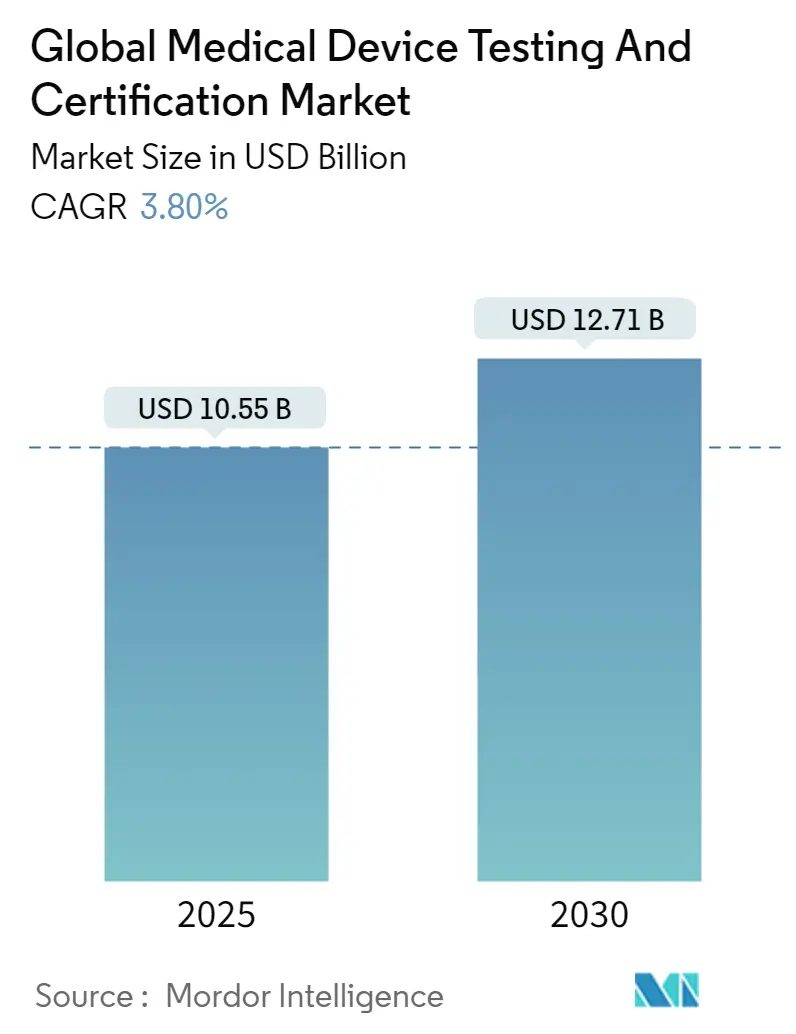
Der Markt für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen erreichte einen Wert von 10,55 Milliarden USD im Jahr 2025 und wird voraussichtlich 12,71 Milliarden USD bis 2030 erreichen, mit einem Wachstum von 3,8% CAGR über den Zeitraum. Die Nachfrage wird durch die gleichzeitige Durchsetzung der EU-Medizinprodukteverordnung (MDR) und des Cybersicherheitsmandats der US-amerikanischen Food and Drug Administration (FDA) geprägt, die beide den Validierungsumfang und die Dokumentationstiefe erweitern. Mittlere Risiko-Klasse-II-Geräte dominieren die Compliance-Volumina, während sich vermehrende KI/ML-Algorithmen und vernetzte Heimdiagnostik neuartige Testprotokolle einführen, die die Premium-Service-Nachfrage ankurbeln. Nordamerika bleibt der Umsatzführer, obwohl Asien-Pazifik die schnellste Laborexpansion verzeichnet, da China und Indien 2024 nationale Gerätegesetze verschärften, was ausländische und inländische Produzenten dazu veranlasste, komplexe Assays auszulagern. Marktteilnehmer mit multi-jurisdiktionellen Akkreditierungen profitieren von anhaltenden Kapazitätsengpässen bei EU-benannten Stellen, die seit 2023 die Vorlaufzeiten verdoppelt haben. Nachhaltigkeitsaudits, angetrieben von europäischen öffentlichen Beschaffungsregeln, und End-to-End-Cybersicherheitsbewertungen entwickeln sich zu Differenzierungsmerkmalen, die es Laboren ermöglichen, höhere Margen für integrierte Aufträge zu verlangen.
Wichtige Erkenntnisse des Berichts
- Nach Dienstleistungsart - Prüfdienstleistungen erfassten 56,56% des Marktanteils für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen im Jahr 2024; Software- und Cybersicherheitsprüfung wird voraussichtlich mit 5,2% CAGR bis 2030 expandieren.
- Nach Geräteklasse - Klasse-II-Geräte machten 43,34% der Marktgröße für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen im Jahr 2024 aus; das Untersegment führte den Umsatz an und wird voraussichtlich eine 5,7% CAGR zwischen 2025-2030 verzeichnen.
- Nach Prüfart - Sterilität & Mikrobiologie beherrschten 37,45% Anteil der Marktgröße für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen im Jahr 2024; Cybersicherheitsprüfung ist das am schnellsten wachsende Untersegment mit 6,1% CAGR.
- Nach Geographie - Nordamerika hielt 38,95% Umsatzanteil im Jahr 2024, während Asien-Pazifik voraussichtlich die höchste 6,7% CAGR bis 2030 verzeichnen wird.
Trends und Erkenntnisse des globalen Marktes für Medizinprodukte-Prüfung und -Zertifizierung
Treiber-Auswirkungsanalyse
| Treiber | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| EU MDR und aktualisierte FDA Safer Devices Act Anforderungen | +1.2% | EU & Nordamerika | Mittelfristig (2-4 Jahre) |
| Schnelle Aufnahme von KI/ML-fähigen Medizinprodukten | +0.8% | Nordamerika & EU, Ausweitung nach Asien-Pazifik | Langfristig (≥ 4 Jahre) |
| Anstieg bei Heimanwendung und tragbaren Diagnostika | +0.6% | Global; am stärksten in Nordamerika & Asien-Pazifik | Kurzfristig (≤ 2 Jahre) |
| Obligatorische Cybersicherheits-Vorab-Markteinreichungen | +0.5% | Nordamerika, Übertragung auf EU | Kurzfristig (≤ 2 Jahre) |
| Nachhaltigkeitsgebundene Beschaffungskriterien | +0.3% | EU zuerst, globale Einführung | Langfristig (≥ 4 Jahre) |
| Qualifizierungszertifizierungen für Arbeitskräfte | +0.2% | Entwickelte Märkte | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Regulatorische Verschärfung unter EU MDR und FDA Safer Devices Act
Das MDR-Übergangsfenster 2024-2028 verpflichtet jedes Legacy-Gerät, die CE-Kennzeichnung unter 23 allgemeinen Sicherheits- und Leistungsanforderungen erneut zu beantragen, wodurch sich die Tiefe der technischen Datei für viele Hersteller verdreifacht ec.europa.eu. Gleichzeitig schreibt Abschnitt 524B des Safer Devices Act vor, dass US-Vorab-Markteinreichungen Software Bills of Materials und Schwachstellenmanagementpläne enthalten müssen, wodurch sich die Dokumentation für jedes vernetzte Produkt erweitert. Der kombinierte Effekt löste einen 40%igen Anstieg bei Anträgen benannter Stellen aus und verlängerte durchschnittliche Überprüfungszeiten über 24 Monate hinaus, was Unternehmen dazu veranlasste, größere Validierungspakete an akkreditierte Labore auszulagern.
Anstieg von KI/ML-fähigen Geräten treibt spezialisierte Validierungsbedürfnisse an
Die öffentliche Datenbank der FDA verzeichnete 882 zugelassene KI/ML-Medizinprodukte bis Mai 2024, ein Anstieg von 45% im Jahresvergleich. Jeder Algorithmus erfordert Bias-Erkennung, Datensatzverschiebungsanalyse und Real-World-Performance-Monitoring, Tests, die über klassische Verifizierung hinausgehen. Das EU-KI-Gesetz, das medizinische KI als "hohes Risiko" klassifiziert, erfordert zusätzlich Lebenszyklus-Risikomanagement. Labore, die Algorithmus-Audit-Dienstleistungen anbieten, verlangen daher Premium-Preise, und diese Dienstleistungslinie wird voraussichtlich über das kommende Jahrzehnt zu einer zentralen Umsatzsäule des Marktes für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen werden.
Wachstum von Heim- und tragbaren Diagnostika erweitert Testvolumina
Die pandemieebedingte Verbrauchervertrautheit mit Schnellantigen-Kits beschleunigte die Annahme von vernetzten Glukometern, EKG-Pflastern und Multi-Analyt-Wearables. Regulierungsbehörden bestehen nun auf Gebrauchstauglichkeits- und Human-Factor-Nachweisen, die außerhalb klinischer Umgebungen gesammelt werden, was die Testeinheitszahlen um fast 30% jährlich für hochvolumige Verbrauchergeräte erhöht. Labore, die in der Lage sind, verteilte Benutzerstudien und Umweltstress-Simulationen durchzuführen, ziehen kontinuierliches Geschäft von Marken an, die schnelle globale Markteinführungen suchen, was den Markt für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen stärkt.
Obligatorische Cybersicherheits-Vorab-Markteinreichungen
Seit Oktober 2023 lehnt die FDA 510(k)-Einreichungen ab, denen sichere-by-Design-Dokumentation fehlt, und vernetzte Geräte, die ohne eine Schwachstellenoffenlegungsrichtlinie eingeführt werden, riskieren Importverweigerung. UL 2900-Zertifizierungspfade sind zum de facto Benchmark geworden ul.com. Prüfhäuser, die früh in Penetrationstestbänke investierten, berichten von Projektpipelines, die bis Mitte 2026 ausgebucht sind, was Cybersicherheit als die am schnellsten wachsende Umsatznische innerhalb des Marktes für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen bestätigt.
Hemmnis-Auswirkungsanalyse
| Hemmnis | (~) % Auswirkung auf CAGR-Prognose | Geografische Relevanz | Auswirkungszeitrahmen |
|---|---|---|---|
| Begrenzte Kapazität & lange Vorlaufzeiten bei benannten Stellen | -0.9% | EU hauptsächlich, mit globalen Übertragungseffekten | Kurzfristig (≤ 2 Jahre) |
| Hohe Testkosten für KMU & Start-ups | -0.6% | Global, mit am stärksten betroffenen Schwellenmärkten | Mittelfristig (2-4 Jahre) |
| Knappheit standardisierter Datensätze für KI-Algorithmus-Validierung | -0.4% | Global, mit Nordamerika & EU als Führern bei KI-Annahme | Langfristig (≥ 4 Jahre) |
| Fragmentierte Nachhaltigkeits-Compliance-Anforderungen | -0.3% | Global, mit EU und Nordamerika priorisiert | Mittelfristig (2-4 Jahre) |
| Quelle: Mordor Intelligence | |||
Begrenzte Kapazität & lange Vorlaufzeiten bei benannten Stellen
Nur 43 benannte Stellen bedienen die gesamte EU unter MDR, und Antrags-zu-Zertifizierungs-Verhältnisse übersteigen 4:1. Durchschnittliche Überprüfungszeiten stiegen von 14 Monaten in 2022 auf mehr als 26 Monate bis Ende 2024. Hersteller haben folglich bestimmte niedrigmargige Produkte aus der EU zurückgezogen, was potenzielle Testvolumina verkleinerte und das Wachstum im Markt für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen dämpfte.
Hohe Testkosten für KMU & Start-ups
Umfassende Biokompatibilitäts-, Sterilität-, EMV- und Cybersicherheitspakete treiben selbst grundlegende Klasse-II-Validierungsrechnungen über 500.000 USD, ein Niveau, das venture-finanzierte Start-ups belastet. Obwohl die FDA reduzierte 510(k)-Gebühren für kleine Unternehmen anbietet, decken diese Einsparungen nur Einreichungskosten ab, nicht die Laborarbeit. Viele KMU verschieben Markteinführungen oder schwenken zu Märkten mit leichteren Regulierungen um, was die unmittelbare Servicenachfrage reduziert.
Segmentanalyse
Nach Dienstleistungsart: Prüfdienstleistungen bleiben grundlegend während Cybersicherheit beschleunigt
Prüfdienstleistungen hielten 56,56% des Marktanteils für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen im Jahr 2024, was ihren Status als unvermeidbare regulatorische Eintrittskarte für alle Geräteklassen widerspiegelt. Zertifizierungsdienstleistungen bleiben zurück, da nur EU- und UK-Routen rechtlich Drittparteien-Auditing erfordern, während die USA mehr auf Herstellerselbstbescheinigung setzen. Da Regulierungsbehörden jedoch die Nachmarktüberwachung intensivieren, gewinnen Inspektions- & Auditierungsumsätze an Schwung. Cybersicherheits- und Softwarevalidierung-statistisch noch in Prüfdienstleistungen eingebettet-stellen den schnellsten Umsatzstrom dar und verzeichnen 5,2% CAGR aufgrund der FDA- und Health Canada-Mandate. Labore, die biologische, mechanische und digitale Sicherheitsbänke an einem Ort integrieren, verkürzen die gesamte Durchlaufzeit um bis zu 30%, ermöglichen Premium-Abrechnung und stärken den Wettbewerbsgraben. Folglich verlagert sich der Markt für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen hin zu gebündelten, abonnement-ähnlichen Qualitätssicherungsverträgen, die mehrjährige Umsatzsichtbarkeit sichern.
Fortgesetzte Investitionen in automatisierte Probenvorbereitung und Hochdurchsatz-Analytik haben die direkte Arbeit pro Bericht seit 2022 um fast 10% reduziert und die Betriebsmargen erhöht. Zertifizierungsdienstleistungen, gehemmt durch benannte-Stellen-Knappheit, werden voraussichtlich langsamer mit 2,5% wachsen, bleiben aber unerlässlich für EU-Marktzugang und erhalten einen defensiven Umsatzboden.
Nach Geräteklasse: Komplexitäts-Sweet-Spot hält Klasse II dominant
Klasse-II-Geräte machten 43,34% der Marktgröße für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen im Jahr 2024 aus, da sie hohe Stückzahlen mit strengen Nachweisanforderungen ausbalancieren. Beispiele umfassen Infusionspumpen, motorisierte Rollstühle und viele KI-fähige Bildgebungsgeräte. Unter dem FDA Predetermined Change Control Plan können Entwickler Algorithmen überarbeiten, ohne eine neue 510(k) einzureichen, vorausgesetzt sie validieren Leistungsgrenzen, was effektiv wiederkehrende Testausgaben jedes Mal sichert, wenn ein Modell aktualisiert wird. Klasse-III-Geräte, obwohl zahlenmäßig geringer, liefern Premium-Gebühren aufgrund obligatorischer klinischer Nachweise und Sterilitätssicherungsniveaus von 10^−6. Klasse-I-Volumina migrieren weiterhin in Richtung interne Selbsttests, doch die Cybersicherheitsklausel zieht einige vernetzte Geräte in Drittpartei-Labore. In-vitro-Diagnostika (IVDs) bleiben nach der EU IVDR-Verlängerung der Übergangsfrist bis 2028 eine besondere Wachstumsnische und erhalten erhöhte Zertifizierungsrückstände.
Insgesamt hält der steigende Softwareinhalt in mittleren Risikoprodukten den Markt für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen fest im Klasse-II-Bereich verankert.
Nach Prüfart: Sterilität erhält Umfang; Cybersicherheit treibt Dynamik
Sterilität & Mikrobiologie-Prüfung behielt 37,45% Umsatzanteil im Jahr 2024, unterstützt durch universelle Anwendbarkeit über Implantate, Einwegprodukte und Kombinationsprodukte. ISO 11737-Updates zu schnellen mikrobiellen Methoden ermutigen Labore, in PCR-basierte Plattformen zu investieren, die Zeit-bis-Zertifikat um 2-3 Tage verkürzen. Parallel verzeichnete Cybersicherheitsprüfung das robusteste Wachstum mit 6,1% CAGR, was den gesetzlich vorgeschriebenen Schwenk zu digital vernetzten Geräten widerspiegelt. Elektrische Sicherheit und elektromagnetische Verträglichkeit (EMV) behalten Relevanz, da 100% der neuen Geräte drahtlose Komponenten integrieren. Verpackungs- & Haltbarkeitsassays profitieren von umweltfreundlichen Materialien, die frische Stabilitätsdatensätze erfordern.
Umgekehrt steigt Sterilitätsprüfung mit langsameren 3,1%, fügt aber dennoch fast 0,6 Milliarden USD in absoluten Zahlen über die Prognosespanne hinzu. Da Labore digitale und mikrobiologische Dienstleistungen kreuzen, steigt der durchschnittliche Projektwert und verbessert die Auftragsbuch-Resilienz.
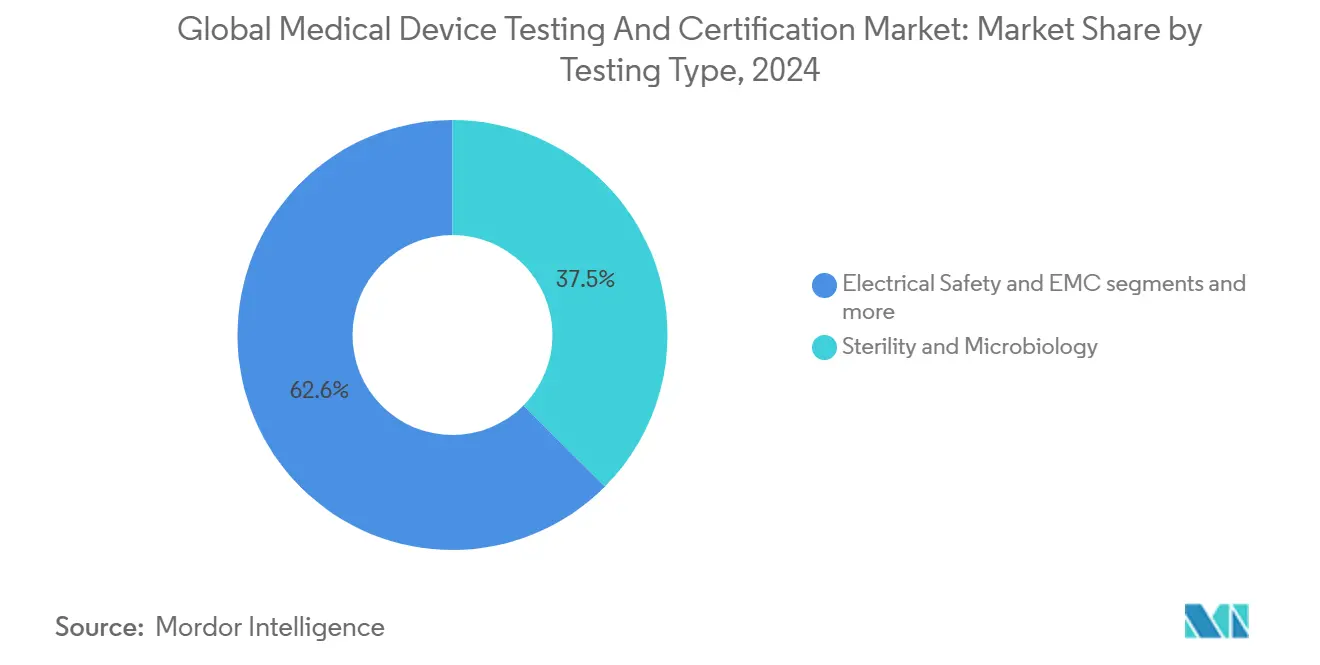
Notiz: Segmentanteile aller einzelnen Segmente verfügbar beim Berichtskauf
Geografieanalyse
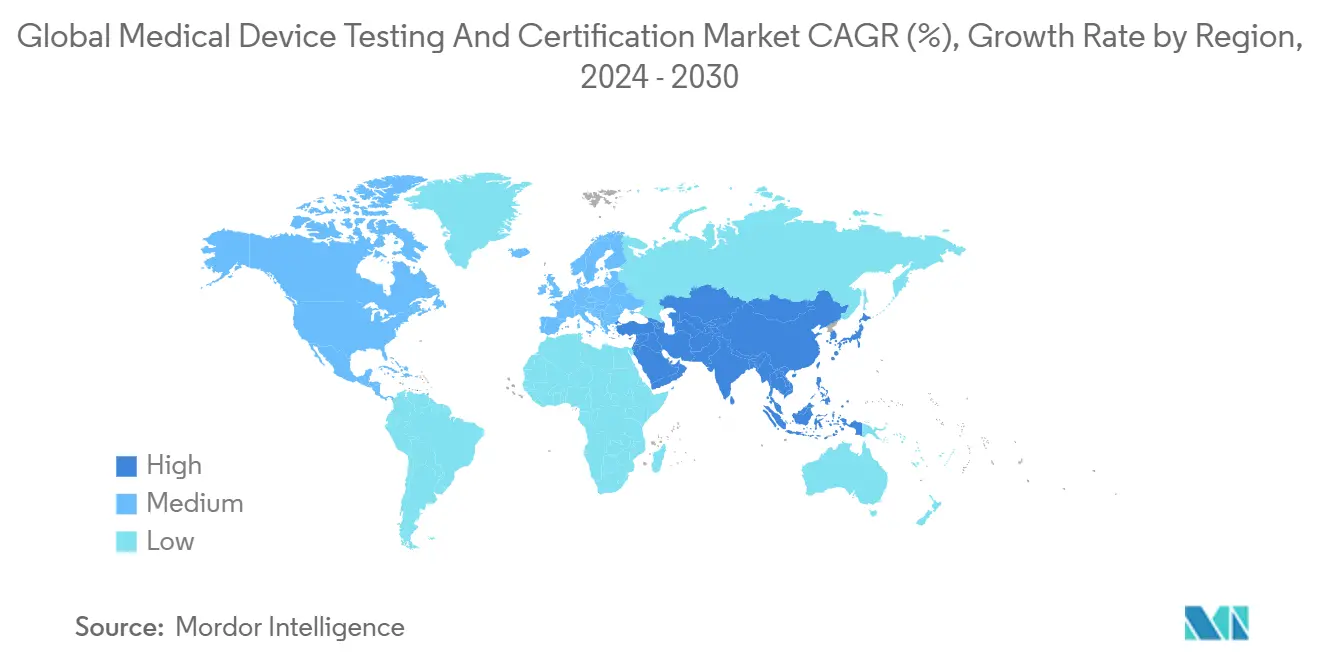
Nordamerika erfasste 38,95% des Marktes für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen im Jahr 2024, verankert durch die FDA-optimierten 510(k)- und Breakthrough Device-Pfade, die kontinuierliche Produkteinführungen katalysieren. Inländische Labore profitieren von tiefen Zahler-Systemen, die Innovation finanzieren, und von einem regulatorischen Umfeld, das explizit mehrere freiwillige Konsensstandards anerkennt und Validierungszyklen verkürzt. Von 2025-2030 ist die Region auf 3,2% CAGR-Expansion eingestellt, langsamer als der globale Durchschnitt aufgrund der Reife.
Asien-Pazifik ist der klare Volumenmotor, prognostiziert auf 6,7% jährliches Wachstum. Chinas aktualisierte Medizinprodukteverordnung, gültig ab Juli 2024, zwingt lokale Produzenten, Drittparteien-Biokompatibilitäts- und Verpackungsdaten zu sichern, was stetige Probenflüsse zu regionalen Laboren antreibt. Indiens Medical Device Rules-Änderung von 2024 erweiterte Drittparteien-Auditanforderungen auf zusätzliche Produktkategorien und fügte schrittweise Nachfrage hinzu. Ausländische Akteure eröffnen schnell Satellitenlabore in Suzhou, Bangalore und Kuala Lumpur, um die steigende Flut zu erfassen.
Europa erlitt kurzfristige Bremse durch benannte-Stellen-Knappheit; sobald sich die Kapazität jedoch normalisiert, werden aufgeschobene Anträge zu abrechnungsfähigen Tests konvertieren und der Region helfen, Schwung nach 2027 wiederzuerlangen. Lateinamerika und der Nahe Osten & Afrika bleiben im Entstehen, profitieren aber von Harmonisierungsinitiativen, die Nachweis der Compliance mit Referenzmarktstandards erfordern-typischerweise ausgeführt von globalen Labornetzwerken.
Wettbewerbslandschaft
Die Wettbewerbslandschaft zeigt moderate Konzentration, mit den Hauptanbietern-SGS SA, Intertek Group plc, Eurofins Scientific SE, TÜV SÜD und UL Solutions. Diese Unternehmen nutzen breite Akkreditierungsportfolios über ISO/IEC 17025, ISO 13485 und mehrere Regulierungsbehörden-Anerkennungen, um Multi-Territorium-Verträge zu gewinnen. SGS erweiterte US-bioanalytische Prüfung im Januar 2025 durch Partnerschaft mit Agilex Biolabs und stärkte seine End-to-End-präklinische bis Nachmarkt-Proposition[1]Quelle: SGS, Outstanding US FDA Inspection Solidifies Position as a Leader in Pharmaceutical Testing in China,
SGS, sgs.com.
Intertek, TÜV SÜD und UL Solutions setzen automatisierte Labormanagementsysteme ein, die Dateneingabefehler reduzieren und Berichtgenerierung beschleunigen und wiederholte Geschäfte mit multinationalen Geräteherstellern sichern, die digitale Rückverfolgbarkeit suchen. Eurofins vertiefte sein medizinisches Portfolio über die Akquisition von Infinity Laboratories im Dezember 2024 und fügte acht US-Einrichtungen hinzu, die auf Mikrobiologie und Verpackungstests spezialisiert sind[2]Quelle: Eurofins Scientific, "Infinity Laboratories Acquisition," eurofins.com . Eine Welle von Mid-Tier-Konsolidierungen-Applus+ kauft Keystone Compliance und Apave akquiriert Baltic Control-signalisiert fortgesetzten Drang nach Größe, um steigende Compliance-Overheads auszugleichen und geografische Abdeckung zu erweitern.
Nischenspezialiaten wie Nelson Labs, BSI Group und Element Materials Technology behalten Hochburg-Positionen in Biokompatibilität, Zertifizierung bzw. EMV. Sie verteidigen Anteile durch tiefe technische Expertise, schnellere Zeit-bis-Terminierung und Nähe zu Innovationszentren. Labor-Automatisierung und KI-verstärkte Analytik verringern jedoch Fähigkeitslücken und ermöglichen größeren Rivalen, in Spezialbereiche einzudringen. Preiskonkurrenz bleibt gedämpft, da regulatorische Komplexität und Kapazitätsengpässe Premium-Abrechnung unterstützen, doch Kunden bevorzugen zunehmend mehrjährige Rahmenvereinbarungen, die Tests über Produktlebenszyklen bündeln, um Rabatte zu sichern.
Führende Unternehmen der globalen Branche für Medizinprodukte-Prüfung und -Zertifizierung
-
Eurofins Scientific
-
SGS SA
-
TÜV SÜD
-
British Standards Institution
-
Intertek Group
- *Haftungsausschluss: Hauptakteure in keiner bestimmten Reihenfolge sortiert
Jüngste Branchenentwicklungen
- Februar 2025: NAMSA und Terumo bildeten eine globale Outsourcing-Partnerschaft zur Beschleunigung der regulatorischen Zulassung von Terumos kardiovaskulären und endovaskulären Geräten, die klinische, Prüf- und Beratungsdienstleistungen abdeckt.
- Januar 2025: SGS startete spezialisierte bioanalytische Dienstleistungen in Nordamerika über Zusammenarbeit mit Agilex Biolabs und verbesserte Discovery- bis Phase-3-Unterstützung für Geräte-Medikament-Kombinationsprodukte.
- Dezember 2024: Eurofins Scientific akquirierte Infinity Laboratories und fügte acht US-Labore hinzu, die sich auf Mikrobiologie-, Chemie- und Verpackungstests für Medizinprodukte konzentrieren
Umfang des globalen Berichts zum Markt für Medizinprodukte-Prüfung und -Zertifizierung
Laut dem Berichtsumfang sind Medizinprodukte-Prüfung, -Zertifizierung und -Auditing notwendig, um die Sicherheit der Geräte zu gewährleisten. Diese Prüfung und Zertifizierung können von Dritten unter anerkannten Auditierungsorganisationen bereitgestellt werden. Der globale Markt für Medizinprodukte-Prüfung und -Zertifizierung ist segmentiert nach Dienstleistungsart (Prüfdienstleistungen, Inspektionsdienstleistungen und Zertifizierungsdienstleistungen), Beschaffungsart (intern und ausgelagert), Geräteklasse (Klasse I, Klasse II und Klasse III), Technologie (aktives implantierbares Medizinprodukt, aktives Medizinprodukt, nicht-aktives Medizinprodukt, In-vitro-Diagnostik-Medizinprodukt, ophthalmisches Medizinprodukt, orthopädisches und dentales Medizinprodukt und andere Technologien) und Geographie (Nordamerika, Europa, Asien-Pazifik, Naher Osten und Afrika und Südamerika). Der Bericht bietet auch Marktgröße und Prognosen für 19 Länder über die Regionen. Der Bericht bietet den Wert (in Millionen USD) für die oben genannten Segmente.
| Prüfdienstleistungen |
| Zertifizierungsdienstleistungen |
| Inspektions- & Auditierungsdienstleistungen |
| Andere |
| Klasse I |
| Klasse II |
| Klasse III |
| In-vitro-Diagnostikgeräte |
| Biokompatibilitätsprüfung |
| Sterilität & Mikrobiologie-Prüfung |
| Elektrische Sicherheit & EMV |
| Software & Cybersicherheitsprüfung |
| Mechanische & physikalische Prüfung |
| Verpackungs- & Haltbarkeitsprüfung |
| Nordamerika | Vereinigte Staaten |
| Kanada | |
| Mexiko | |
| Europa | Deutschland |
| Vereinigtes Königreich | |
| Frankreich | |
| Italien | |
| Spanien | |
| Restliches Europa | |
| Asien-Pazifik | China |
| Indien | |
| Japan | |
| Südkorea | |
| Australien | |
| Restliches Asien-Pazifik | |
| Südamerika | Brasilien |
| Argentinien | |
| Restliches Südamerika | |
| Naher Osten und Afrika | GCC |
| Südafrika | |
| Restlicher Naher Osten und Afrika |
| Nach Dienstleistungsart (Wert) | Prüfdienstleistungen | |
| Zertifizierungsdienstleistungen | ||
| Inspektions- & Auditierungsdienstleistungen | ||
| Andere | ||
| Nach Geräteklasse (Wert) | Klasse I | |
| Klasse II | ||
| Klasse III | ||
| In-vitro-Diagnostikgeräte | ||
| Nach Prüfart (Wert) | Biokompatibilitätsprüfung | |
| Sterilität & Mikrobiologie-Prüfung | ||
| Elektrische Sicherheit & EMV | ||
| Software & Cybersicherheitsprüfung | ||
| Mechanische & physikalische Prüfung | ||
| Verpackungs- & Haltbarkeitsprüfung | ||
| Nach Geographie (Wert) | Nordamerika | Vereinigte Staaten |
| Kanada | ||
| Mexiko | ||
| Europa | Deutschland | |
| Vereinigtes Königreich | ||
| Frankreich | ||
| Italien | ||
| Spanien | ||
| Restliches Europa | ||
| Asien-Pazifik | China | |
| Indien | ||
| Japan | ||
| Südkorea | ||
| Australien | ||
| Restliches Asien-Pazifik | ||
| Südamerika | Brasilien | |
| Argentinien | ||
| Restliches Südamerika | ||
| Naher Osten und Afrika | GCC | |
| Südafrika | ||
| Restlicher Naher Osten und Afrika | ||
Wichtige im Bericht beantwortete Fragen
Wie groß ist der aktuelle Markt für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen?
Die Marktgröße für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen erreichte 10,55 Milliarden USD im Jahr 2025 und wird voraussichtlich auf 12,71 Milliarden USD bis 2030 wachsen.
Welches Dienstleistungssegment hält den größten Anteil?
Prüfdienstleistungen, einschließlich Biokompatibilitäts-, Sterilität- und Cybersicherheitsassays, erfassten 56,56% des Marktanteils für Medizinprodukte-Prüfung & -Zertifizierungsdienstleistungen im Jahr 2024.
Warum sind Klasse-II-Geräte der primäre Umsatztreiber?
Klasse-II-Geräte kombinieren hohe Produktionsvolumina mit moderaten bis hohen regulatorischen Nachweisanforderungen, was sie zur zentralen Nachfragequelle für ausgelagerte Prüfung über den Prognosezeitraum macht.
Wie werden Cybersicherheitsvorschriften das Marktwachstum beeinflussen?
Das FDA-Mandat für Cybersicherheits-Vorab-Markteinreichungen und die weit verbreitete Annahme von UL 2900-Standards treiben eine 6,1% CAGR für Cybersicherheitsprüfdienstleistungen bis 2030 an, schneller als jede andere Testkategorie.
Welche Region wird voraussichtlich am schnellsten wachsen?
Asien-Pazifik wird voraussichtlich eine 6,7% CAGR verzeichnen, dank schärferer regulatorischer Rahmenwerke in China und Indien, die Hersteller zwingen, Drittparteien-Testvolumina zu erhöhen.
Seite zuletzt aktualisiert am: