Markt-Trends von Globales intravenöses Immunglobulin Industrie
Es wird erwartet, dass das Segment Primäre Immundefizienzkrankheiten im Prognosezeitraum eine hohe CAGR verzeichnen wird
Es wird erwartet, dass das Segment der primären Immundefizienzkrankheiten (PIDs) einen erheblichen Marktanteil halten wird
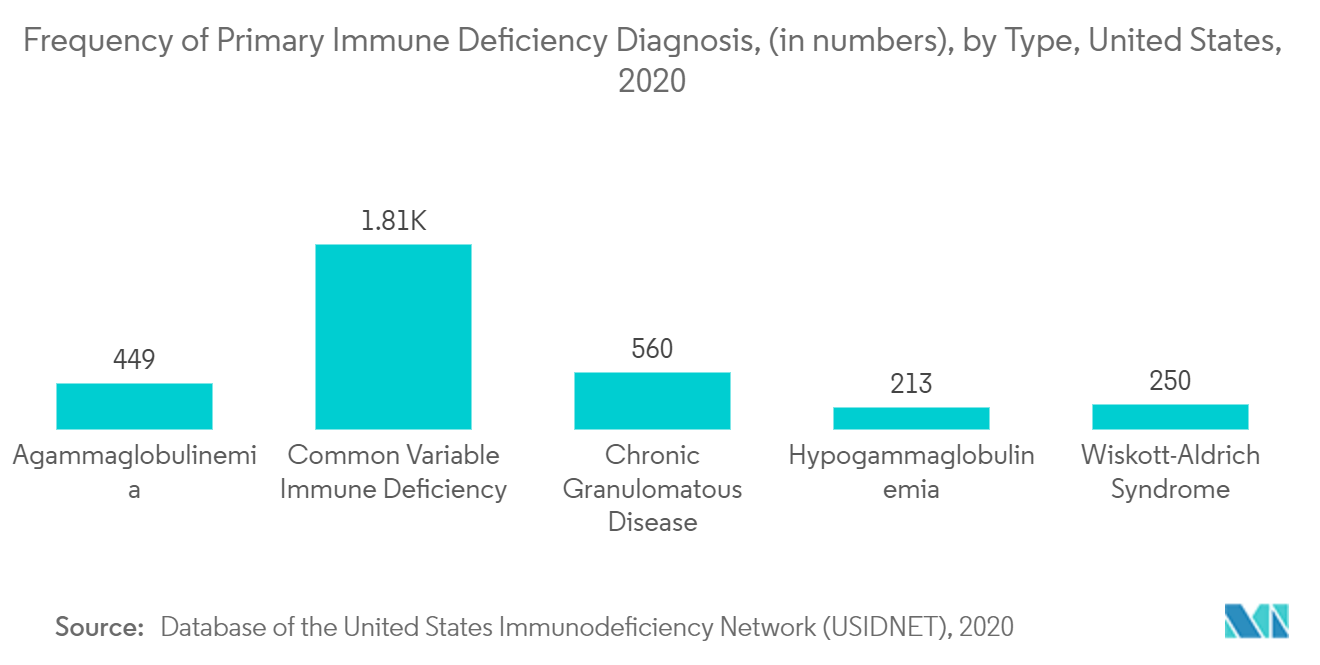
Die intravenöse Immunglobulin-Therapie (IVIG) wird in den letzten Jahren hauptsächlich zur Behandlung primärer Immundefizienzerkrankungen (PIDs) und anderer Immundefizienzerkrankungen eingesetzt. Für Menschen mit PID mit Antikörpermangel, der für mehr als die Hälfte der primären Immundefekte verantwortlich ist, stehen mehrere spezifische medizinische Therapien zur Verfügung. Diese Krankheiten, wie z. B. die häufige variable Immunschwäche (CVID), die X-chromosomale Agammaglobulinämie (XLA) und andere Erkrankungen, sind durch einen Mangel an und/oder eine beeinträchtigte Antikörperfunktion gekennzeichnet. Die hohe Belastung durch primäre Immundefizienz ist ein wesentlicher Faktor für das Wachstum des Segments. Laut dem Forschungsartikel mit dem Titel Systematic Review of Primary Immunodeficiency Diseases in Malaysia 1979-2020, der im August 2020 in Frontiers in Immunology veröffentlicht wurde, wird beispielsweise davon ausgegangen, dass weltweit etwa sechs Millionen Menschen mit PIDs leben, davon nur 27.000 -60.000 Fälle wurden diagnostiziert. Der oben genannten Quelle zufolge lag die Inzidenz von PIDs in Singapur bei 2,65 pro 100.000 Lebendgeburten, wobei die geschätzte Häufigkeit bei einer von 37.000 Lebendgeburten liegt. Außerdem gibt es laut einem Update der Centers for Disease Control and Prevention (CDC) vom April 2020 mehr als 400 Arten primärer Immundefekte mit unterschiedlichem Schweregrad. Somit spiegeln diese Statistiken den steigenden Bedarf an Immunglobulinen zur Behandlung von Immundefizienzerkrankungen wider. Daher wird erwartet, dass die wachsende Belastung durch PIDs weltweit das Wachstum des untersuchten Segments im Prognosezeitraum vorantreiben wird
Darüber hinaus beschäftigen sich mehrere Pharmaunternehmen mit der Entwicklung von Immunglobulinprodukten zur Behandlung primärer Immundefizienz. Beispielsweise berichtete GC Pharma im Mai 2021, dass die US-amerikanische Food and Drug Administration (FDA) den Biologics License Application (BLA) des Unternehmens für GC5107 (Immune Globulin Intravenous (Human), 10 % Liquid) für die Behandlung angenommen hat der primären humoralen Immunschwäche, einer Klasse vererbter genetischer Störungen, die dazu führen, dass eine Person ein schwächeres oder fehlendes Immunsystem hat
Aufgrund der Verfügbarkeit von IVIG-Therapien und der Fortschritte bei intravenösen Immunglobulinprodukten zur Behandlung der weit verbreiteten primären Immunschwächekrankheiten wird daher erwartet, dass das untersuchte Segment in den kommenden Jahren erheblich wachsen wird
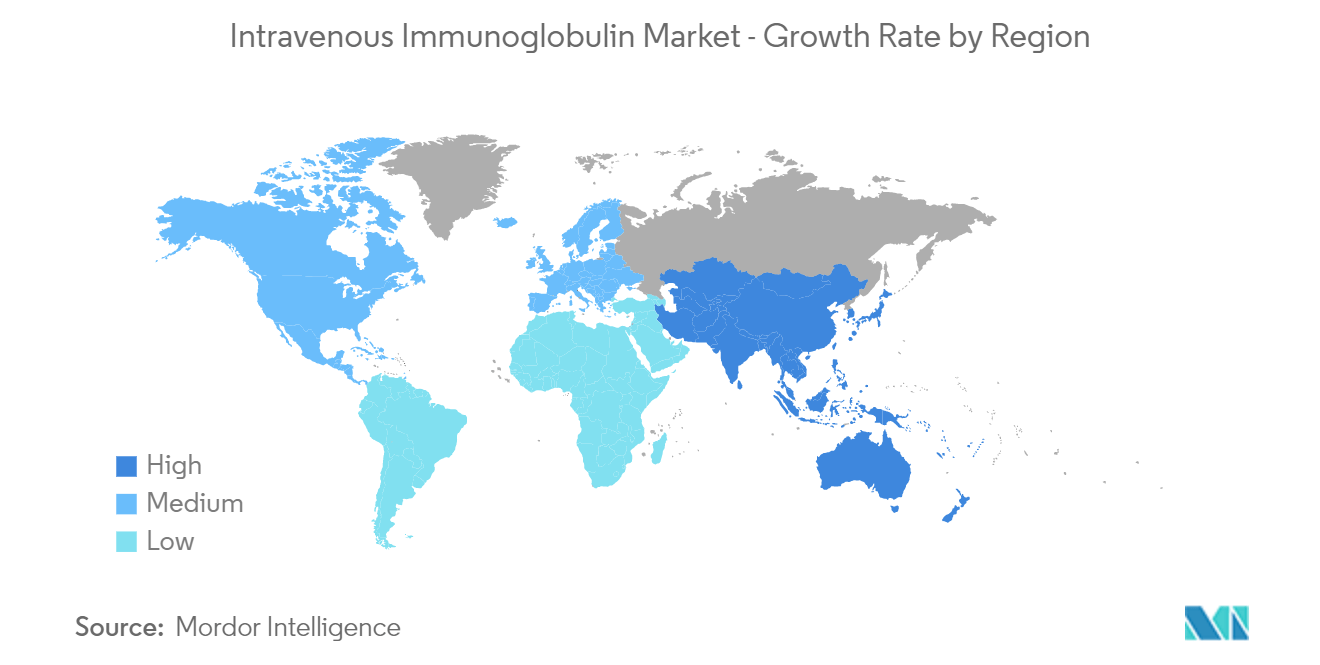
Es wird erwartet, dass Nordamerika im Prognosezeitraum den Markt dominieren wird
Es wird erwartet, dass die Vereinigten Staaten einen großen Marktanteil in Nordamerika halten werden. Die wichtigsten Faktoren, die das Marktwachstum im Land vorantreiben, sind ein entwickeltes und gut strukturiertes Gesundheitssystem; ein wachsender Fokus auf Forschung und Entwicklung; und die starke Präsenz der Marktteilnehmer
Darüber hinaus wird erwartet, dass die wachsende Belastung durch Zielkrankheiten wie primäre Immunschwächekrankheiten in der Region das Marktwachstum ankurbeln wird. Beispielsweise wurden nach Angaben des National Institute of Allergy and Infectious Diseases im Jahr 2020 in den Vereinigten Staaten mehr als 400 verschiedene PID-Typen diagnostiziert, was mehr als 500.000 amerikanische Bevölkerungsgruppen betrifft, die von PIDs betroffen sind. Darüber hinaus lag laut USIDNET-Register im Jahr 2020 die Häufigkeit schwerer kombinierter Immundefizienz (SCID) in der amerikanischen Bevölkerung bei 355. Darüber hinaus wird erwartet, dass die zunehmenden Forschungs- und Entwicklungsaktivitäten und die schnellen Produktzulassungen das Marktwachstum für intravenöses Immunglobulin vorantreiben werden Region
Darüber hinaus meldete Emergent BioSolutions Inc., ein multinationales spezialisiertes biopharmazeutisches Unternehmen mit Sitz in den Vereinigten Staaten, im August 2021 den Beginn einer klinischen Phase-III-Studie zur Bewertung seines aus Plasma gewonnenen SARS-CoV-2-Immunglobulins intravenös (COVID-HIG). Therapie als mögliche ambulante Behandlung für Patienten mit Coronavirus (COVID-19), bei denen ein hohes Risiko für das Fortschreiten einer schweren Erkrankung besteht
Darüber hinaus erhielt Pfizer im Februar 2021 die Genehmigung der US-amerikanischen Food and Drug Administration für den ergänzenden Biologics License Application (sBLA), der für PANZYGA, ein intravenöses Immunglobulin (IVIg) zur Behandlung erwachsener Patienten mit chronisch entzündlicher demyelinisierender Polyneuropathie (CIDP), eingereicht wurde
Daher wird erwartet, dass der Markt im Prognosezeitraum aufgrund der oben genannten Faktoren ein deutliches Wachstum verzeichnen wird