Markt-Trends von Behandlung des Hunter-Syndroms Industrie
Es wird erwartet, dass das Segment der Enzymersatztherapie (ERT) im Prognosezeitraum ein deutliches Wachstum auf dem Markt für die Behandlung des Hunter-Syndroms verzeichnen wird
Es wird erwartet, dass die Enzymersatztherapie im Prognosezeitraum ein deutliches Wachstum auf dem Markt für die Behandlung des Hunter-Syndroms verzeichnen wird, da die Verfügbarkeit von Enzymersatztherapien, das zunehmende Bewusstsein und die weniger strengen Richtlinien für seltene Krankheiten zunehmen
Die Enzymersatztherapie (ERT) ist ein Behandlungsstandard für verschiedene Arten seltener Krankheiten und besteht darin, das mangelhafte oder fehlende Enzym durch eine funktionsfähige rekombinante Version durch intravenöse Verabreichung zu ersetzen. Beispielsweise wurde in einem im Oktober 2021 veröffentlichten Artikel beobachtet, dass Pabinafusp alfa sowohl gegen die somatischen als auch gegen die ZNS-Symptome von Patienten mit MPS-II wirksam war, da es die Blut-Hirn-Schranke passieren kann, um das zentrale Nervengewebe zu erreichen. Daher wird erwartet, dass die hohe Wirksamkeit und Sicherheit des neuartigen Enzymmedikaments seine Akzeptanz bei der Behandlung von Patienten mit Hunter-Syndrom erhöhen und damit das Marktwachstum vorantreiben wird
Laut einem im Mai 2021 in PLOS One veröffentlichten Artikel wurde beobachtet, dass die Enzymersatztherapie (ERT) die primäre Behandlung für Mukopolysaccharidose Typ II (Hunter-Syndrom) ist, die durch Reduzierung der somatischen Symptome zur Verbesserung des Krankheitsverlaufs beiträgt , einschließlich Hepatomegalie und Splenomegalie. Darüber hinaus gilt laut derselben Quelle die ERT unter Verwendung intravenös verabreichter humaner rekombinanter Iduronat-2-sulfatase als aktueller Behandlungsstandard für Patienten mit Hunter-Syndrom. Daher wird erwartet, dass solche Studien die Nachfrage nach ERT steigern und das Wachstum des Segments im Prognosezeitraum vorantreiben werden
Die zunehmende Entwicklung von Enzymersatztherapieprodukten durch Unternehmen dürfte auch die Verfügbarkeit von ERT-Therapien auf dem Markt erhöhen und so das Wachstum weiter steigern. Beispielsweise hat das MHLW im März 2021 IZCARGO (Pabinafusp alfa 10 ml, intravenöse Tropfinfusion) für die Behandlung von MPS II in Japan zugelassen. Es handelt sich um eine rekombinante Iduronat-2-Sulfatase-Enzymersatztherapie (ERT), die mithilfe von J-Brain Cargo, einer von JCR entwickelten proprietären Technologie, entwickelt wurde, um Therapeutika über die Blut-Hirn-Schranke (BBB) zu verabreichen
Aufgrund der hohen Wirksamkeit und Sicherheit von ERT, der steigenden Zahl von Forschungsstudien und zunehmenden Produktzulassungen wird daher erwartet, dass das untersuchte Segment im Prognosezeitraum wächst
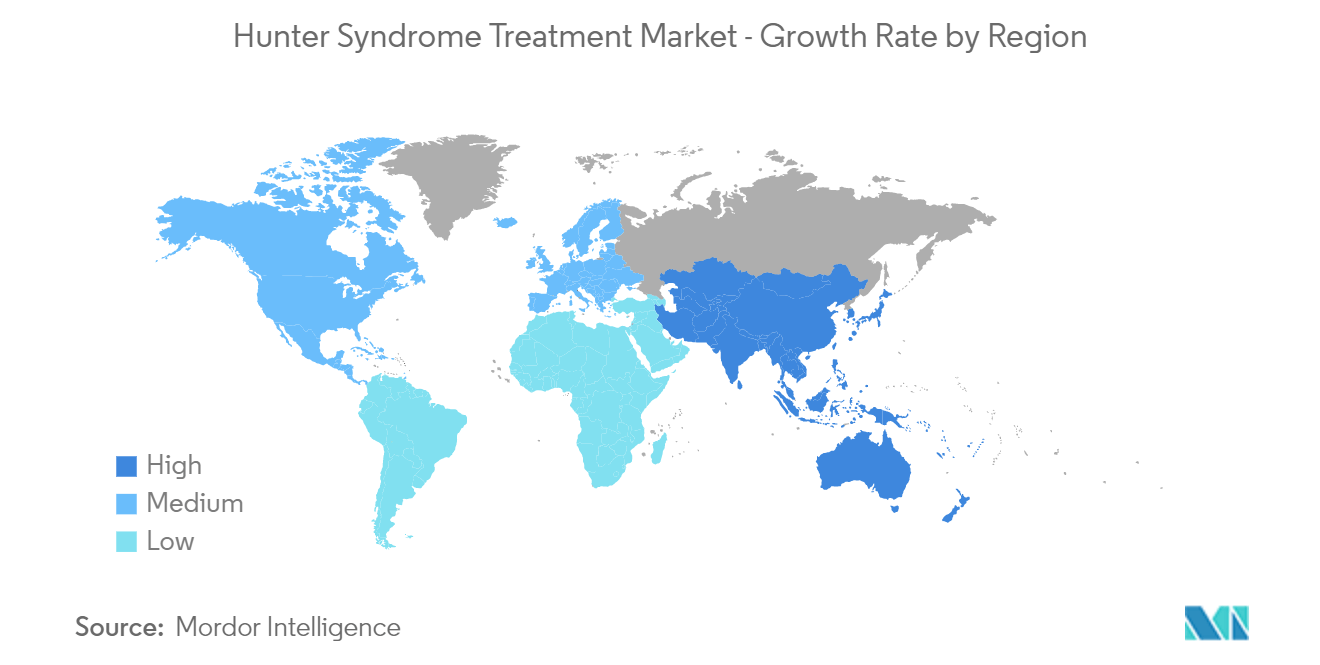
Es wird erwartet, dass Nordamerika im Prognosezeitraum einen erheblichen Anteil am Markt für die Behandlung des Hunter-Syndroms halten wird
Für Nordamerika wird im Prognosezeitraum aufgrund des steigenden Bewusstseins für seltene Krankheiten, günstiger Vorschriften für die Entwicklung von Arzneimitteln für seltene Leiden, wachsender Gesundheitsausgaben und günstiger Erstattungsrichtlinien für teure Medikamente in der Region ein gesundes Wachstum erwartet. Das Vorhandensein einer gut etablierten Gesundheitsinfrastruktur, die zunehmende Einführung neuartiger Therapien und technologische Fortschritte dürften auch den Markt für die Behandlung des Hunter-Syndroms ankurbeln
Es wird erwartet, dass der zunehmende Fokus der Unternehmen auf die Entwicklung fortschrittlicher Produkte sowie die steigenden Produkteinführungen und -zulassungen in der Region den Markt im Prognosezeitraum ankurbeln werden. Beispielsweise gab REGENXBIO Inc. im August 2022 seine Pläne bekannt, im Jahr 2024 einen Biologics License Application (BLA) einzureichen und dabei den beschleunigten Zulassungsweg der FDA für RGX-121 zur Behandlung von Mukopolysaccharidose Typ II (MPS II) zu nutzen. Im Februar 2022 präsentierte Homology Medicines, Inc. auf dem jährlichen WorldSymposium Meeting Daten zum Gentherapiekandidaten HMI-203 zur Behandlung des Hunter-Syndroms (MPS II) im Rahmen einer klinischen Phase-I-Dosiseskalationsstudie bei Erwachsenen mit Hunter-Syndrom
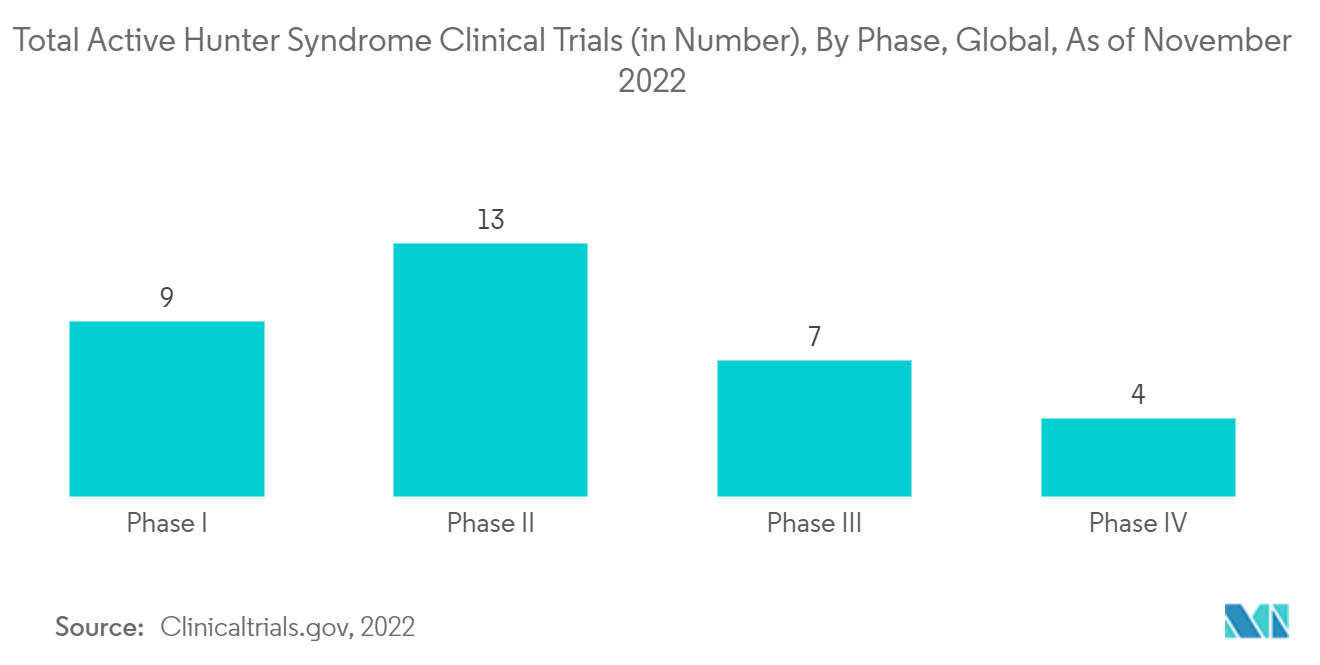
Der zunehmende Fokus wichtiger Akteure auf die Durchführung klinischer Studien zur Bewertung der Sicherheit und Wirksamkeit von Enzymmedikamenten und -therapien zur Behandlung von Patienten mit Hunter-Syndrom könnte ebenfalls zum Wachstum des Marktes beitragen. Laut Clinicaltrials.gov führte REGENXBIO Inc. beispielsweise im September 2022 eine klinische Studie der Phase II/III durch, um die Sicherheit und Wirksamkeit von RGX-121, einer Gentherapie, bei Kindern ab fünf Jahren mit schwerem MPS zu bestimmen II. Laut derselben Quelle laufen in den Vereinigten Staaten derzeit 23 aktive klinische Studien zum Hunter-Syndrom, davon neun in klinischen Studien der Phase I, zehn in Phase II, drei in Phase III und eine in Phase IV. Daher könnte die hohe Anzahl klinischer Studien im Land das Wachstum des Marktes für die Behandlung des Hunter-Syndroms im Prognosezeitraum ankurbeln
Der zunehmende Fokus auf die Entwicklung verschiedener sicherer Behandlungsmöglichkeiten für Patienten mit Hunter-Syndrom und zunehmende Produkteinführungen im Land dürften das Marktwachstum im Prognosezeitraum ankurbeln