Markt-Trends von Behandlung der Duchenne-Muskeldystrophie Industrie
Es wird erwartet, dass das Exon-Skipping-Segment im Prognosezeitraum einen großen Marktanteil halten wird
Interne Deletionen im Gen für Dystrophin, ein Protein, das für die Erhaltung der Integrität der Muskelzellmembranen entscheidend ist, sind die Hauptursache für Duchenne-Muskeldystrophie. Eine mögliche therapeutische Strategie besteht darin, ein Exon in der Nähe der Stelle zu maskieren, an der die anderen fehlen, damit die verbleibenden Exons zusammenkommen können. Exon-Skipping ist eine der wirksamsten Behandlungsstrategien zur Wiederherstellung der Expression eines verkürzten, aber funktionellen Dystrophin-Proteins
Darüber hinaus konzentrieren sich die Marktteilnehmer auf häufige Markteinführungen der Exon-Skipping-Technologie, die ein wesentlicher Treiber des Segments ist und so das Marktwachstum vorantreibt. Beispielsweise gab Novartis im Juni 2022 bekannt, dass die Europäische Kommission (EK) Tabrecta (Capmatinib) als Monotherapie zur Behandlung von Erwachsenen mit fortgeschrittenem nicht-kleinzelligem Lungenkrebs (NSCLC) zugelassen hat, der Mutationen aufweist, die Exon 14 (METex14) verursachen. Überspringen und die eine systemische Therapie benötigen, nachdem sie zuvor eine Immuntherapie und/oder eine platinbasierte Chemotherapie erhalten haben. Ebenso gab Sarepta Therapeutics, Inc. im Februar 2021 bekannt, dass die US-amerikanische Food and Drug Administration (FDA) AMONDYS 45 (Casimersen) zugelassen hat. AMONDYS 45 ist ein Antisense-Oligonukleotid aus Sareptas Phosphordiamidat-Morpholino-Oligomer (PMO)-Plattform, das für die Behandlung der Duchenne-Muskeldystrophie (DMD) bei Patienten mit einer bestätigten Mutation, die für das Exon-45-Skipping geeignet ist, indiziert ist
Aufgrund von Produkteinführungen und technologischen Fortschritten wird daher im Prognosezeitraum ein erhebliches Segmentwachstum erwartet
Für die Region Nordamerika wird im Prognosezeitraum ein beträchtliches Wachstum erwartet
Es wird erwartet, dass die nordamerikanische Region aufgrund neuer Produktinnovationen, hoher Gesundheitsausgaben und staatlicher Sensibilisierungsprogramme erheblich wachsen wird. Aufgrund der gestiegenen Krankheitsprävalenz und der erwarteten Markteinführung attraktiver Pipeline-Kandidaten haben die Vereinigten Staaten den regionalen Markt angeführt und werden diese Position voraussichtlich behalten. Darüber hinaus wird erwartet, dass der Markt wächst, da weltweit, insbesondere in den Vereinigten Staaten, mehr klinische Studien durchgeführt werden. Beispielsweise erhielt Elamipretide im Mai 2022 vom Office of Orphan Products Development der US-amerikanischen Food and Drug Administration (FDA) den Orphan Drug Designation zur Behandlung von Patienten mit Duchenne-Maskulärer Dystrophie (DMD). In ähnlicher Weise genehmigte die FDA im Februar 2021 Amondys 45 (Casimersen injizierbar) von Sarepta Therapeutics, ein Antisense-Oligonukleotid, zur Behandlung von Menschen mit Duchenne-Muskeldystrophie. Darüber hinaus erhielt die Injektion von Viltepso (Viltolarsen) im August 2020 eine beschleunigte Zulassung von der US-amerikanischen Food and Drug Administration zur Behandlung der Duchenne-Muskeldystrophie (DMD) bei Patienten, die eine nachgewiesene Mutation des DMD-Gens haben, die für Exon-53-Skipping anfällig ist. Daher wird erwartet, dass solche Faktoren das Marktwachstum in der nordamerikanischen Region vorantreiben werden
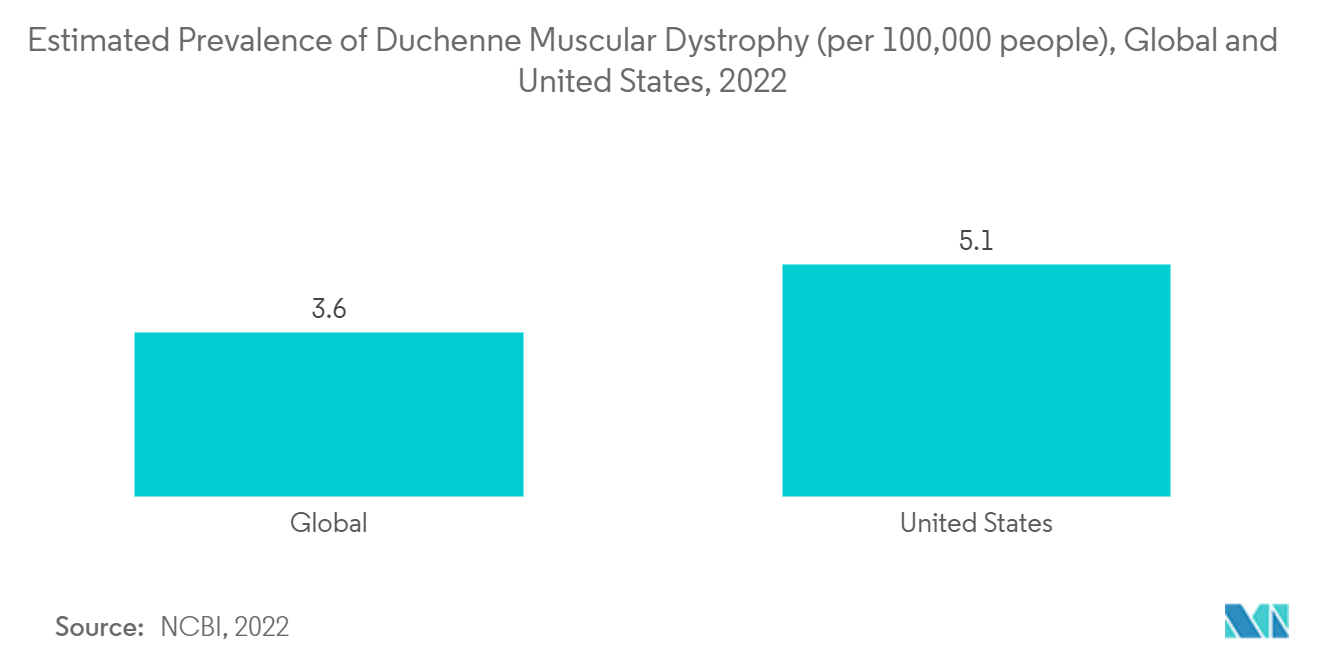
Es wird erwartet, dass der Markt für die Behandlung von Duchenne-Muskeldystrophie in den Vereinigten Staaten aufgrund des großen ungedeckten Bedarfs und positiver Initiativen der Hauptakteure erheblich wachsen wird. Beispielsweise kündigte Pfizer Inc. im April 2022 Pläne zur Eröffnung der ersten Standorte in den USA für die Phase-3-Studie an, die die experimentelle Mini-Dystrophin-Gentherapie, Fordadistrogene Movaparvovec, bei ambulanten Patienten mit Duchenne-Muskeldystrophie (DMD) evaluiert. Marktschätzungen für die DMD-Erkrankung zufolge dürften darüber hinaus in den kommenden Jahren Pipeline-Medikamente den Markt erobern, wodurch sich der Marktanteil von Exon-Skipping-Therapien verdreifachen und der Marktanteil von Steroiden um die Hälfte sinken wird. Acht neue Medikamente in der Pipeline, die hohen Preise für Gen- und Zelltherapien sowie der erwartete Anstieg der Behandlungsraten werden wesentliche Wachstumstreiber für den DMD-Markt sein. Daher wird in den USA im Prognosezeitraum mit einem deutlichen Anstieg des Marktwachstums gerechnet